Unterschied zwischen Stickstoff und Nitrat
Der Schlüsselunterschied Zwischen Stickstoff und Nitrat ist das Stickstoff ist ein Element, während Nitrat eine Verbindung von Stickstoff und Sauerstoff ist.
Nitrate sind hoch verfügbare anionische Formen, die Stickstoff enthalten. Natürlich existiert Stickstoff als Gas und es ist das Hauptreservoir des Stickstoffs. Pflanzen können diesen gasförmigen Stickstoff nicht direkt verwenden, sodass einige Bakterien dazu neigen. Der atmosphärische Stickstoff wird durch industrielle Fixierung, durch die Wirkung des Blitzes und durch einige der Bodenmikroorganismen in Nitrat umgewandelt. Wir nennen diesen Prozess Stickstofffixierung. Ammoniak und Nitriten können auch durch die nitrifizierenden Bakterien im Boden in Nitrat umgewandelt werden. Die Nitrate im Boden werden dann von Pflanzen für ihre Aktivitäten absorbiert. Darüber hinaus können Bodennitrate durch die Denitrifizierbakterien wie Thiobacillus Denitrificans in Stickstoffgas umwandeln.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Stickstoff
3. Was ist Nitrat
4. Seite an Seitenvergleich - Stickstoff gegen Nitrat in tabellarischer Form
5. Zusammenfassung
Was ist Stickstoff?
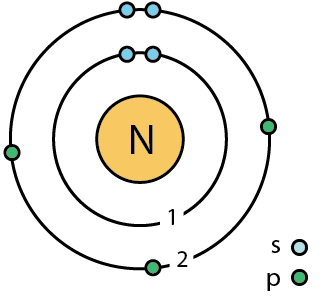
Stickstoff ist das vierthäufigste Element in unserem Körper. Es befindet sich in Gruppe 15 der Periodenzüchter mit der Atomzahl 7. Stickstoff ist ein Nichtmetall und seine Elektronenkonfiguration ist 1S2 2S2 2p3. Das P-Orbital ist halb gefüllt, wodurch Stickstoff die Möglichkeit bietet, drei weitere Elektronen einzunehmen, um die stabile Edelgaskonfiguration zu erreichen. Daher ist Stickstoff dreifellos.

Abbildung 01: Stickstoffatom
Zwei Stickstoffatome können eine dreifache Bindung zwischen ihnen bilden und jeweils drei Elektronen bilden. Dieses Diatommolekül befindet sich bei Raumtemperatur in der Gasphase und bildet ein farbloses, geruchloses und geschmackloses Inertgas. Stickstoff ist ein nicht entzerrbares Gas und unterstützt keine Verbrennung. Dies ist das am häufigsten vorkommende Gas in der Erdatmosphäre (ca. 78%).
Natürlich gibt es zwei Isotope Stickstoff, N-14 und N-15. N-14 ist häufiger. Bei sehr niedrigen Temperaturen geht Stickstoff in den flüssigen Zustand. Es ähnelt dem Aussehen des Wassers, aber die Dichte ist niedriger als Wasser.
Stickstoff ist in der chemischen Industrie weithin nützlich und eine wichtige Komponente, die für lebende Organismen erforderlich ist. Die wichtigste kommerzielle Verwendung von Stickstoff ist die Verwendung als Rohstoff für Ammoniak, Salpetersäure, Harnstoff und andere Stickstoffverbindungen. Diese Verbindungen können in Düngemittel eingebaut werden, da Stickstoff eines seiner Hauptelemente ist, die Pflanzen für ihr Wachstum benötigen. Stickstoff ist auch an Orten wichtig, an denen wir eine inerte Umgebung benötigen, insbesondere bei chemischen Reaktionen. Darüber hinaus ist flüssiger Stickstoff wichtig, um die Dinge sofort und als Kühlmittel in verschiedenen Geräten einzufrieren (e.G.: Computers).
Was ist Nitrat?
Nitrat ist ein Polyatomanion, das Stickstoff und drei Sauerstoffatome enthält. Das Stickstoffatom befindet sich im +5 Oxidationszustand. Die Geometrie dieses Moleküls ist trigonaler Planar und zeigt auch Resonanz. Dieses einwertige Anion kann sich jeder anderen Art von Kation verbinden, um verschiedene organische und anorganische Verbindungen zu bilden.
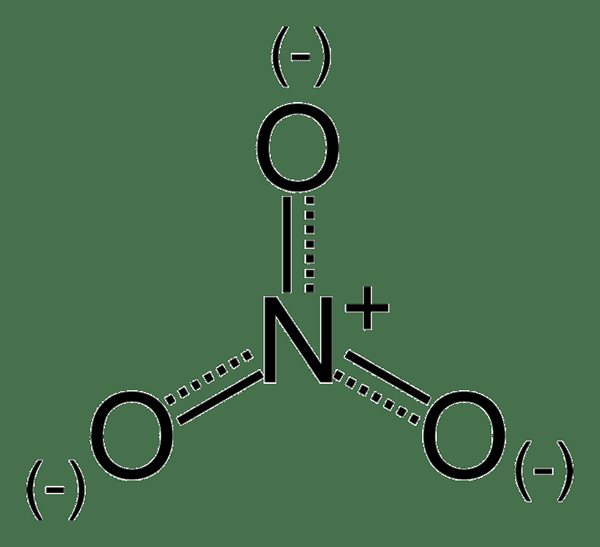
Abbildung 02: stabilisierte Resonanzstruktur des Nitratanions
Nitrat-haltige Verbindungen sind häufig wasserlöslich und in der Natur in der Natur in Boden, Wasser und Nahrung reichlich vorhanden. Nitrate sind in erster Linie wichtig, um Düngemittel zu machen. Sie sind auch wichtig, um Sprengstoffe zu machen. Nitrate sind relativ ungiftig. In unserem Körper konvertieren Nitrate in Nitriten und daher kann es giftig werden.
Was ist der Unterschied zwischen Stickstoff und Nitrat?
Obwohl die Begriffe Stickstoff und Nitrat ähnlich klingen, sind sie sehr unterschiedliche Begriffe. Der Schlüsselunterschied zwischen Stickstoff und Nitrat besteht darin, dass Stickstoff ein Element ist, während Nitrat eine Verbindung von Stickstoff und Sauerstoff ist. Mit anderen Worten, Stickstoff ist das chemische Element mit der Atomzahl 7 und Symbol N, während Nitrat ein Anion mit der chemischen Formel Nr. Ist3-. Darüber hinaus ist ein Stickstoffatom tribelig, während Nitratanion einwertig ist. Bei der Betrachtung der Ladung ist das freie Stickstoffatom neutral, während Nitratanion -1 Ladung hat. Darüber hinaus ist der Oxidationszustand des freien Stickstoffatoms Null, aber bei Nitratanion +5.

Zusammenfassung -Stickstoff gegen Nitrat
Stickstoff ist das chemische Element mit der Atomzahl 7 und Symbol N und Nitrat ist ein Anion mit der chemischen Formel NO3-. Der Schlüsselunterschied zwischen Stickstoff und Nitrat besteht darin, dass Stickstoff ein Element ist, während Nitrat eine Verbindung von Stickstoff und Sauerstoff ist.
Referenz:
1. Powlson, d.S., und T.M. Addiscott. „Stickstoff in Böden | Nitrate.”Enzyklopädie von Böden in der Umwelt, 2005, PP. 21-31., doi: 10.1016/B0-12-348530-4/00905-X.
Bild mit freundlicher Genehmigung:
1. "7 Stickstoff (N) BOHR -Modell" von Ahazard.ScienceWriter - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia
2. "Nitrat-Ion" von Benjah-BMM27-eigene Arbeit (Public Domain) über Commons Wikimedia


