Unterschied zwischen P -Alkalinität und M -Alkalinität
Schlüsselunterschied - p Alkalinität gegen M -Alkalinität
Der Begriff Alkalinität bezieht sich auf die Menge einer wässrigen Lösung, die zur Neutralisierung der durch eine Säure verursachten Säure erforderlich ist. Obwohl die Alkalität mit der Basizität einer wässrigen Lösung wie Wasser, Blut usw. zusammenhängt., Es misst den Widerstand der Lösung gegenüber den pH -Veränderungen aufgrund des Vorhandenseins einer Säure. Die Hauptionen, die zur Alkalität von Wasser beitragen, sind Hydroxylionen (OH-), Carbonationen (co32-) und Bicarbonat -Ionen (HCO3-). Die Alkalinität wird gemäß dem Endpunkt, angegeben, wenn eine wässrige Grundlösung mit einer Säure titriert wird, in drei Gruppen eingeteilt. Ätzende Alkalinität, P -Alkalinität und M -Alkalinität sind diese Kategorien. Dieser Artikel konzentriert sich auf den Unterschied zwischen P -Alkalinität und M -Alkalinität. Die Namen P -Alkalinität und M -Alkalinität sind je nach Indikator angegeben, der im Titrationsprozess verwendet wird. Der Schlüsselunterschied zwischen palkalinität und m alkalinität ist das P -Alkalinität bestimmt die Alkalität des gesamten Hydroxyls und die Hälfte des Carbonat wohingegen m Alkalinität bestimmt die Alkalität aller Hydroxyl, Carbonat und Bicarbonat. Malkalität wird als allgemeine oder Gesamtalkalität angesehen, da Carbonatspezies eine wichtige Rolle bei der Gesamtalkalität von Wasser spielen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist palkalinität
3. Was ist M -Alkalinität?
4. Seite für Seitenvergleich - P -Alkalinität gegen M -Alkalinität in tabellarischer Form
5. Zusammenfassung
Was ist palkalinität?
Der Begriff palkalinität steht für “Phenolphthalein - Alkalität”. Es ist die Messung des Hydroxids (OH-) und Carbonation (co3-2) Menge. Es wird durch Titrieren einer Wasserprobe mit einer Säure einer bekannten Konzentration in Gegenwart von Phenolphthalein als Indikator bestimmt. Um zu verstehen, was in dieser Titration passiert, ist es wichtig, über die Dissoziation von Kohlensäure zu wissen.

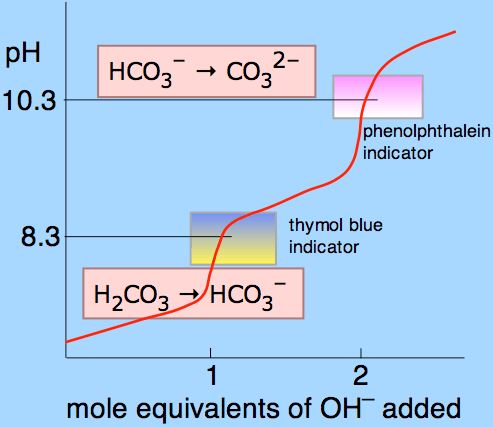
Abbildung 01: Titrationskurve für Kohlensäure unter Verwendung von Phenolphthalein und Thymolblau als Indikatoren.
Die obige Kurve zeigt, was während der Titration von Kohlensäure passiert. Es ist eine diprotische Säure und kann zwei Wasserstoffatome entfernen, die als Protonen bezeichnet werden. Der obere Teil der Kurve zeigt an, dass die Carbonat- und Hydroxylionenmenge im pH -Bereich von Phenolphthalein angegeben ist. Seit dem pH -Bereich, in dem Phenolphthalein die Farbänderung ergibt.3 - 10.0, die P -Alkalinität wird in diesem pH -Bereich gemessen. Hier wird die folgende Beziehung verwendet, um die Alkalität dieser bestimmten Stichprobe zu erklären, die für die Titration verwendet wird.
1 ml Säure = 1 meq/l Alkalinität
Was ist M -Alkalinität??
Die Gesamtmessung von Hydroxid (OH-), Bicarbonat (HCO3-) und Carbonat (co32-) Die Ionenmenge wird durch M -Alkalinität angegeben. Der Buchstaben M bezieht sich auf Methylorange. Es ist der Indikator, der verwendet wird, um die Gesamtalkalität zu bestimmen, die durch die oben genannten Hydroxid- und Carbonatspezies angegeben ist. Wenn Methylorange zugesetzt wird, gibt es seine Farbänderung nur in seinem pH -Bereich, der 3 ist, 3.1 - 4.4. Da nur Spurenkonzentrationen anderer Säuren in Wasser gelöst sind, mit Ausnahme von Kohlensäure -Säure, kann die Alkalinität als Gesamtalkalität angesehen werden, da sie die gesamte Carbonatalkalität ergibt.
Was ist der Unterschied zwischen palkalinität und m alkalinität?
P -Alkalinität gegen M Alkalinität | |
| P -Alkalität ist die Messung der Alkalität durch Hydroxidionen und die Hälfte der Carbonatalkalität. | M -Alkalinität ist die Messung der Alkalität durch Hydroxidionen und Gesamtkarbonatalkalität. |
| Indikator | |
| Phenolphthalein -Indikator wird verwendet, um die P -Alkalinität zu bestimmen. | Methylorange wird verwendet, um die Alkalinität zu bestimmen. |
| pH -Bereich | |
| Die Alkalinität wird in einem Bereich von 8 gemessen.3 - 10.0 Ph. | Die Alkalinität wird in einem pH -Bereich von 3 gemessen.1 - 4.4. |
| Carbonatspezies | |
| p Alkalinität bestimmt hauptsächlich OH- und Hco3- Spezies. | M Alkalinität bestimmt oh-, HCO3- und co32- Spezies. |
Zusammenfassung -P -Alkalinität gegen M -Alkalinität
Durch die Messung der P -Alkalinität und der M -Alkalinität kann man die Menge des in der Probe gelösten Gesamtkohlenstoffs berechnen. Eine Reihe von Säuren sind natürlich in Wasser gelöst, jedoch in Spurenkonzentrationen. Carbonsäure findet sich jedoch in hohen Konzentrationen, weil CO2 kann sich in Wasser auflösen. Daher ist die Gesamtalkalität des Wassers häufig gleich der Karbonatalkalität. Der Hauptunterschied zwischen P -Alkalinität und M -Alkalinität besteht darin, dass die P -Alkalinität die Messung der Alkalität durch Hydroxidionen und die Hälfte der Carbonatalkalinität ist, während die Alkalinität der Alkalinität die Messung der Alkalinität durch Hydroxidionen und Gesamtkarbonatalkalität ist.
Laden Sie die PDF -Version von P alkalinity vs m alkalinität herunter
Sie können die PDF -Version dieses Artikels herunterladen und ihn für Offline -Zwecke gemäß Zitatnotizen verwenden. Bitte laden Sie die PDF -Version hier den Unterschied zwischen p alkalinität und m alkalinität herunter.
Referenz:
1.Titration einer schwachen polyprotischen Säure.”Libre Textchemie. N.P., 6. Januar. 2016. Netz. Hier verfügbar. 5. Juni 2017.
Bild mit freundlicher Genehmigung:
1. "Titcurve H2CO3" von langsamer - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia


