Unterschied zwischen Phosgen und Diphosgen
Der Schlüsselunterschied Zwischen Phosgene und Diphosgen ist das Phosgen hat ein Kohlenstoffatom, ein Sauerstoffatom und zwei Chloratome, während Diphosgen die Anzahl all dieser Atome doppelt so.
Phosgen und Diphosgen sind organische Verbindungen. Beide Verbindungen enthalten Kohlenstoff-, Sauerstoff- und Chloratome. Die Anzahl jeder Atometyp im Diphosgenmolekül ist genau die doppelte Anzahl dieser Atome im Phosgenmolekül.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Phosgene
3. Was ist Diphosgen
4. Ähnlichkeiten zwischen Phosgen und Diphosgen
5. Seite an Seitenvergleich - Phosgen gegen Diphosgen in tabellarischer Form
6. Zusammenfassung
Was ist Phosgene?
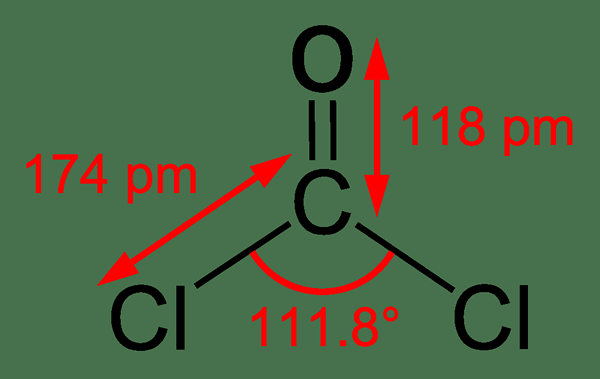
Phosgen ist eine organische Verbindung mit der chemischen Formel cocl2. Es ist ein farbloses Gas, und es hat einen Geruch ähnlich wie frisch geschnittenes Gras. Obwohl es im Wasser unlöslich ist, kann es mit Wasser reagieren. Darüber hinaus verfügt es über eine trigonale planare Geometrie, und der Cl-C-C-C-CL-Bindungswinkel ist 111.8 °. Diese Verbindung ist ein einfaches Acylchlorid, das sich aus Kohlensäure bildet.

Abbildung 01: Die chemische Struktur des Phosgenmoleküls
In der industriellen Skala produzieren wir Phosgen, indem wir reines Kohlenmonoxid und Chlorgas durch Aktivkohlenstoff bestehen. Hier ist Aktivkohlenstoff der Katalysator. Darüber hinaus ist diese Reaktion exotherm, und wir müssen den Reaktor während der Reaktion abkühlen. Bei der Betrachtung der Verwendung von Phosgene können wir es bei der Herstellung von Isocyanaten, in der Synthese von Carbonaten usw. verwenden, usw.
Was ist Diphosgen?
Diphosgen ist eine organische Verbindung mit der chemischen Formel C2Ö2Cl4. Es ist eine farblose Flüssigkeit bei Raumtemperatur. Es ist ein wichtiges Reagenz bei organischen Synthesereaktionen. Im Vergleich dazu weist DiPhosgen eine geringe Toxizität als Phosgen auf. Diese Flüssigkeit sollte jedoch sorgfältig behandelt werden als Phosgene, was ein Gas ist.
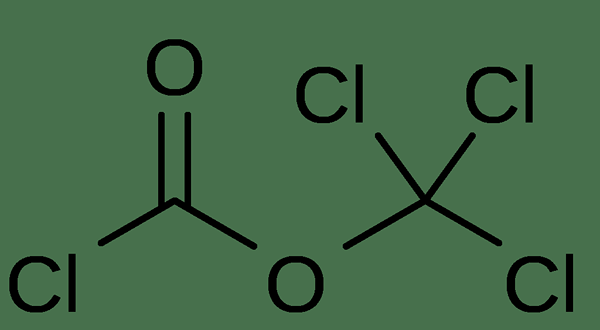
Abbildung 02: Die chemische Struktur des Diphosgenmoleküls
Wir können Diphosgen im Labor durch radikale Chlorierung von Methylchloroformat herstellen. Diese Reaktion erfordert das Vorhandensein einer UV -Strahlungsquelle. Abgesehen davon kann eine radikale Chlorierung von Methylformiat auch Diphosgen bilden. Darüber hinaus wandelt sich Diphosgen in Phosgen um, wenn sie erhitzt oder bei Reaktion mit Holzkohle.
Was sind die Ähnlichkeiten zwischen Phosgen und Diphosgen?
- Phosgen und Diphosgen sind organische Verbindungen.
- Beide Verbindungen enthalten Kohlenstoff-, Sauerstoff- und Chloratome.
- Diese Verbindungen sind in Wasser unlöslich.
Was ist der Unterschied zwischen Phosgen und Diphosgene?
Phosgen ist eine organische Verbindung mit der chemischen Formel cocl2 Während Diphosgen eine organische Verbindung mit der chemischen Formel C ist2Ö2Cl4. Der Schlüsselunterschied zwischen Phosgen und Diphosgen besteht darin, dass Phosgen ein Kohlenstoffatom, ein Sauerstoffatom und zwei Chloratome aufweist.
Phosgen tritt als farbloses Gas mit einem Geruch auf, das dem von frisch geschnittenem Gras ähnelt, während Diphosgen als farblose Flüssigkeit bei Raumtemperatur auftritt. Im Vergleich dazu ist Diphosgen weniger toxisch als Phosgene, muss jedoch sorgfältig behandelt werden. Darüber.
Die folgende Tabelle fasst den Unterschied zwischen Phosgen und Diphosgen zusammen.
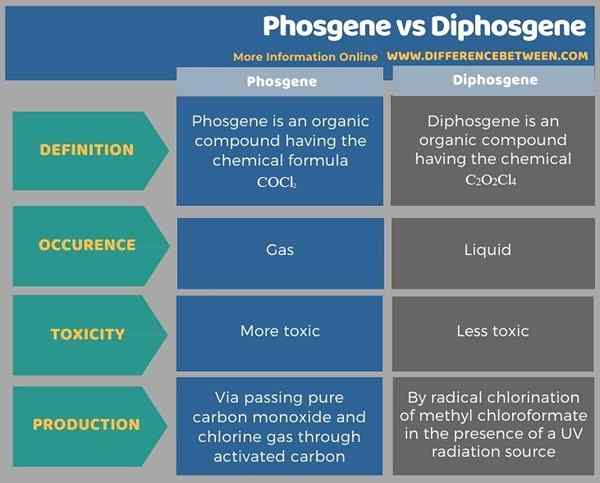
Zusammenfassung -Phosgen gegen Diphosgene
Phosgen und Diphosgen sind organische Verbindungen. Beide Verbindungen enthalten Kohlenstoff-, Sauerstoff- und Chloratome. Der Schlüsselunterschied zwischen Phosgen und Diphosgen besteht darin, dass Phosgen ein Kohlenstoffatom, ein Sauerstoffatom und zwei Chloratome aufweist.
Referenz:
„Diphosgen.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 6. Dezember. 2011, hier erhältlich.
„Diphosgen.”DiPhosgene - Ein Überblick | Sciencedirect -Themen, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Phosgen-Dimensions-2D" von Phosgen-Dimensions-2D.PNG: Ben Millsssvg-Version: N-REVEN-Phosgen-Dimensionen-2d.PNG (Public Domain) über Commons Wikimedia
2. "Diphosgene Struktur" von Ed (Edgar181) - eigene Arbeit (Public Domain) über Commons Wikimedia


