Unterschied zwischen Kaliumacetat und Kaliumchlorid

Der Schlüsselunterschied Zwischen Kaliumacetat und Kaliumchlorid ist das Kaliumacetat ist das Kaliumsalz von Essigsäure, während Kaliumchlorid ein Metallhalogenidsalz ist, das Kalium- und Chloridionen enthält.
Kaliumacetat und Kaliumchlorid sind Salzverbindungen und ionische Verbindungen, die Kaliumionen enthalten, kombiniert mit Anionen Acetat bzw. Chlorid. Kaliumacetat ist eine spezielle Form von Kaliumsalz, die in Krankenhäusern selten verwendet wird, aber Kaliumchlorid ist in Krankenhäusern ein übliches Medikament.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Kaliumacetat
3. Was ist Kaliumchlorid
4. Seite an Seitenvergleich - Kaliumacetat gegen Kaliumchlorid in tabellarischer Form
5. Zusammenfassung
Was ist Kaliumacetat?
Kaliumacetat ist das Kaliumsalz von Essigsäure. Es hat die chemische Formel ch3Kochen, in dem k+ ist Kaliumkation und ch3GURREN- ist Acetatanion. Darüber hinaus beträgt die Molmasse dieser Verbindung 98.14 g/mol. Es erscheint als weißes kristallines Pulver. Darüber hinaus ist diese Substanz grellig. Der Schmelzpunkt beträgt 292 ° C, und bei weiterer Erhitzen zersetzt sich die Verbindung.
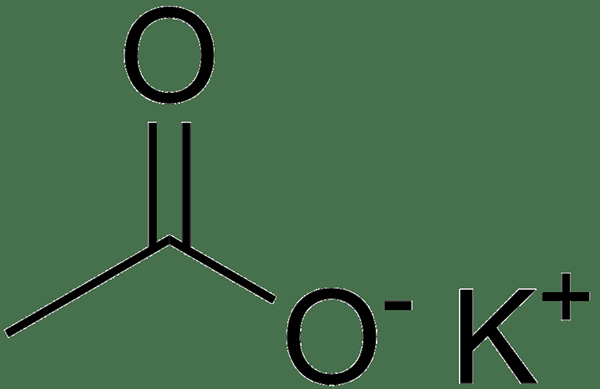
Abbildung 01: Struktur von Kaliumacetat
Darüber hinaus können wir Kaliumacetat durch die Behandlung einer Kalium-haltigen Base mit Essigsäure vorbereiten. Es ist eine Säure-Base-Neutralisationsreaktion. Zu den häufigsten Basen gehören Kaliumhydroxid und Kaliumcarbonat.
Darüber hinaus gibt es viele Anwendungen von Kaliumacetat. Wir können es als Deicer verwenden, um die Bildung von Eis zu verhindern. Außerdem ist es als Feuerlöschmittel nützlich. Außerdem ist es auch ein Lebensmittelzusatz und wird für die Erhaltung von Lebensmitteln verwendet. Obwohl es Anwendungen in der Medizin hat, ist die Verwendung dieser Verbindung in Krankenhäusern selten.
Was ist Kaliumchlorid?
Kaliumchlorid ist eine ionische Verbindung, die Kaliumkationen und Chloridanionen enthält. Es ist ein Metallhalogenidsalz mit der chemischen Formel KCL. Die Verbindung erscheint als farblose Glaskristalle und löst sich leicht in Wasser auf, wodurch sich in Ionen dissoziiert. Darüber hinaus hat die wässrige Lösung einen salzigen Geschmack.

Abbildung 02: Kaliumchlorid
In Bezug auf die Nützlichkeit ist diese Verbindung in der Landwirtschaft als Kaliumrich-Dünger nützlich. Es hat auch medizinische Anwendungen, insbesondere zur Behandlung niedriger Blutkaliumspiegel. Darüber hinaus ist es als chemischer Ausgangsmaterial für die Synthese von Kaliumhydroxid und Kaliummetall sehr nützlich.
Was ist der Unterschied zwischen Kaliumacetat und Kaliumchlorid?
Kaliumacetat und Kaliumchlorid sind ionische Verbindungen aus Kationen und Anionen. Der wichtigste Unterschied zwischen Kaliumacetat und Kaliumchlorid besteht darin. Ein weiterer Unterschied zwischen Kaliumacetat und Kaliumchlorid ist ihr Aussehen. Kaliumacetat erscheint als weißes kristallines Pulver, während Kaliumchlorid als farblose vitreöse Kristalle erscheint.

Zusammenfassung -Kaliumacetat gegen Kaliumchlorid
Kaliumacetat und Kaliumchlorid sind im Grunde ionische Verbindungen aus Kationen und Anionen. Der wichtigste Unterschied zwischen Kaliumacetat und Kaliumchlorid besteht darin.
Referenz:
1. „Tödliche Injektionen: Kaliumchlorid gegen. Kaliumacetat.” com, Oklahoman, 11. Oktober. 2015, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Kaliumacetat -Skelett" von Edgar181 (Diskus
2. "Kaliumchlorid" (Public Domain) über Commons Wikimedia


