Unterschied zwischen S- und P -Blockelementen
Schlüsselunterschied -s vs. P -Blockelemente
Der Schlüsselunterschied Zwischen S- und P -Blockelementen können am besten mit ihrer elektronischen Konfiguration erklärt werden. In den S -Blockelementen füllt sich das letzte Elektronen in der S -Unterschale und in P -Blockelementen, das letzte Elektron. Wenn sie Ionen bilden; S Blockelemente entfernen ihre Elektronen aus der äußersten S-Unterschale leicht, während P-Blockelemente Elektronen an die P-Unterschale akzeptieren oder Elektronen aus der P-Subshell entfernen. Einige Elemente in der P-Gruppe bilden positive Ionen, die Elektronen aus der äußersten P-Subshell entfernen, und einige Elemente (die elektronegativsten Elemente) bilden negative Ionen, die ein Elektron von anderen akzeptieren. Wenn Sie die chemischen Eigenschaften berücksichtigen, gibt es einen signifikanten Unterschied zwischen S- und P -Blockelementen. Dies ist im Grunde auf die Elektronenkonfiguration zurückzuführen.
Was sind S-Blockelemente?
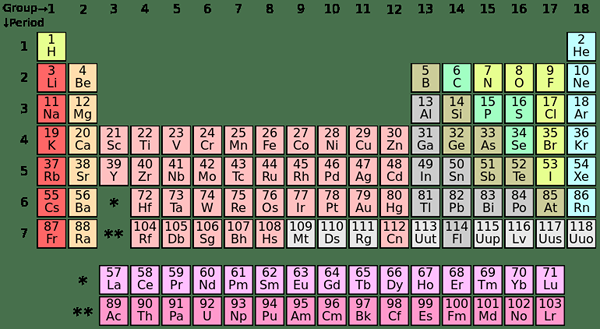
S-Blockelemente sind die chemischen Elemente in Gruppe I und Gruppe II in der Periodenzüchtertabelle. Da S -Unterschale nur zwei Elektronen aufnehmen kann, haben diese Elemente normalerweise eine (Gruppe I) oder zwei (Gruppe II) Elektronen in der äußersten Hülle. Die Elemente in Gruppe I und II sind oben in der Tabelle angezeigt.
| Ia | Ii a | |
| 2 | Li | Sei |
| 3 | N / A | Mg |
| 4 | K | Ca |
| 5 | Rb | Sr |
| 6 | CS | Ba |
| 7 | Fr | Ra |
| Ia | Alkali Metalle |
| Ii a | Alkalische Erdmetalle |
Alle Elemente in S-Block bilden positive Ionen und sind sehr reaktiv.

Die Platzierung der S-Block-Elemente in der Periodenzüchtertabelle
Was sind P-Block-Elemente?
P-Blockelemente sind die Elemente, deren letzte Elektron. Es gibt drei P-Orbitale; Jedes Orbital kann zwei Elektronen aufnehmen und insgesamt sechs P-Elektronen herstellen. Daher haben P-Block-Elemente ein bis sechs P-Elektronen in ihrer äußersten Hülle. P-Block enthält sowohl Metalle als auch Nichtmetalle; Außerdem gibt es auch einige Metalloiden.
| 13 | 14 | 15 | 16 | 17 | 18 | |
| 2 | B | C | N | Ö | F | Ne |
| 3 | Al | Si | P | S | Cl | Ar |
| 4 | Ga | Ge | Als | Se | Br | Kr |
| 5 | In | Sn | Sb | Te | ICH | Xe |
| 6 | Tl | Pb | Bi | Po | Bei | Rn |
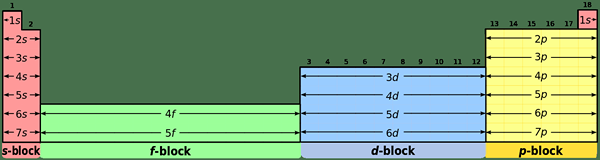
Was ist der Unterschied zwischen S- und P -Blockelementen?
Gemeinsame Elektronenkonfiguration:
S-Blockelemente: S-Blockelemente haben die gemeinsame Elektronenkonfiguration von [Noble Gas] ns1 (für Gruppe I Elemente) und [Noble Gas] ns2 (für Elemente der Gruppe II).
P-Blockelemente: P-Blockelemente haben die gemeinsame Elektronenkonfiguration von [Noble Gas] ns2 np1-6. Aber Helium hat 1s2 Aufbau; Es ist eine besondere Situation.
Oxidationszustände:
S-Blockelemente: S-Blockelemente zeigen keine mehreren Oxidationszustände wie P-Block-Elemente. Beispielsweise zeigen die Elemente der Gruppe I +1 Oxidationszustand und die Elemente der Gruppe II zeigen einen Oxidationszustand von +2.
P-Blockelemente: Im Gegensatz zu den S-Block-Elementen haben P-Block-Elemente einen gemeinsamen Oxidationszustand für ihre jeweilige Gruppe in der Periodenzüchttabelle und einige andere zusätzliche Oxidationszustände abhängig von der Stabilität des Ions.
| Gruppe | 13 | 14 | 15 | 16 | 17 | 18 |
| Allgemeine Elektronenkonfiguration | ns2np1 | ns2np2 | ns2np3 | ns2np4 | ns2np5 | ns2np6 |
| 1st Mitglied der Gruppe | Sei | C | N | Ö | F | Er |
| Häufige Oxidationszahl | +3 | +4 | +5 | -2 | -1 | 0 |
| Andere Oxidationszustände | +1 | +2, -4 | +3, -3 | +4, +2, | +3, +5, +1, +7 | - |
Eigenschaften:
S-Blockelemente: Im Allgemeinen sind alle S-Block-Elemente Metalle. Sie sind glänzende, gute Elektro- und Wärmeleiter und leicht zu entfernen Elektronen aus der Valenzschale. Sie sind die reaktivsten Elemente in der Periodenzüchtertabelle.
P-Blockelemente: Die meisten P-Block-Elemente sind Nichtmetalle. Sie haben niedrige Siedepunkte, schlechte Leiter und schwierig, Elektronen aus der äußersten Hülle zu entfernen. Stattdessen gewinnen sie Elektronen. Einige der Nichtmetalle sind Feststoffe (C, P, S, SE) bei Raumtemperatur, während einige Gase (Sauerstoff, Stickstoff) sind. Brom ist ein Nichtmetall und eine Flüssigkeit bei Raumtemperatur.
Zusätzlich enthält P-Block einige metallische Elemente; Aluminium (Al), Gallium (GA), Indium (in), Zinn (SN), Thallium (TL), Blei (PB) und Wismut (Bi).
Bild mit freundlicher Genehmigung:
1. "Periodenziehungstabelle (Polyatomisch)" durch Depiep [CC BY-SA 3.0] über Commons
2. "Periodenzüchter blockiert SPDF (32 Spalte)" durch Benutzer: Depiep [CC BY-SA 3.0] über Commons


