Unterschied zwischen Salzbrücke und Wasserstoffbrückenbindung
Der Schlüsselunterschied Zwischen Salzbrücke und Wasserstoffbrücke ist das Die Salzbrücke ist ein Röhrchen mit einem Elektrolyt, der zwei halbe Zellen in einer elektrochemischen Zelle verbindet, während Wasserstoffbindung eine Anziehungskraft zwischen zwei Atomen von zwei verschiedenen Molekülen ist.
Die Salzbrücke ist sehr nützlich, um die Konnektivität zwischen zwei halben Zellen einer elektrochemischen Zelle aufrechtzuerhalten. Es ist für das bloße Auge sichtbar. Die Wasserstoffbindung ist jedoch eine chemische Bindung, die die Konnektivität zwischen zwei Molekülen aufrechterhält, die Wasserstoffbrückenbindungen bilden können.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist eine Salzbrücke
3. Was ist eine Wasserstoffbindung
4. Seite an Seite Vergleich - Salzbrücke gegen Wasserstoffbrückenbindung in tabellarischer Form
5. Zusammenfassung
Was ist eine Salzbrücke?
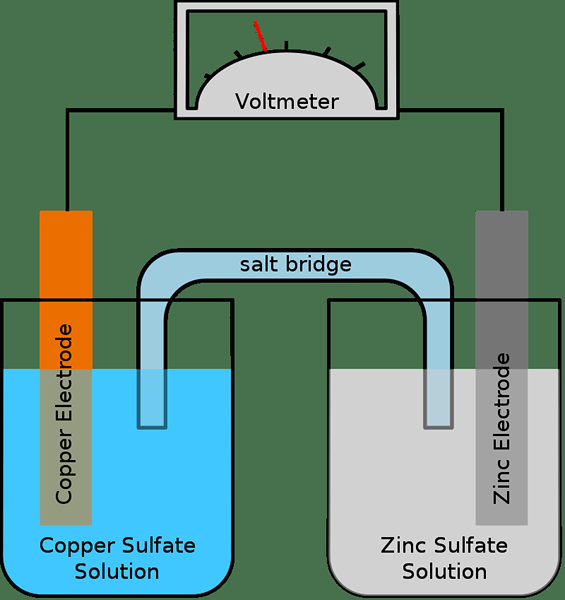
Salzbrücke ist ein Röhrchen, das einen Elektrolyten enthält (typischerweise in Form eines Gels), der einen elektrischen Kontakt zwischen zwei Lösungen bietet. Daher ist dieses Rohr wichtig, um die Oxidation und Reduktionsreaktionen der galvanischen Zelle zu verbinden. Der Zweck einer Salzbrücke besteht darin, die elektrochemische Reaktion schnell das Gleichgewicht zu erleichtern. Wenn es keine Salzbrücke gibt, sammelt eine halbe Zelle positive Ladungen, und die andere Halbzelle sammelt negative Ladungen an. Folglich stoppt die Stromerzeugung.
Es gibt zwei Haupttypen von Salzbrücken: Glasrohrbrücke und Filterpapierbrücke. Die Glasrohr-Salzbrücke ist ein U-Stuhl aus Glas und enthält den Elektrolyten. In der Filterpapiersalzbrücke befindet sich ein Filterpapier mit dem Elektrolyten eingeweicht.
Was ist Wasserstoffbindung?
Eine Wasserstoffbindung ist eine Art Anziehungskraft zwischen zwei Atomen von zwei verschiedenen Molekülen. Es ist eine schwache Anziehungskraft. Im Vergleich zu anderen Arten von intramolekularen Kräften wie polarpolaren Wechselwirkungen, nichtpolaren nichtnonpolaren Wechselwirkungen wie Vander Waal-Kräften ist die Wasserstoffbindung stärker.
Normalerweise bilden Wasserstoffbrückenbindungen zwischen polaren kovalenten Molekülen. Diese Moleküle enthalten polare kovalente Bindungen, die sich aufgrund der Differenz der Elektronegativitätswerte der Atome, die sich in der kovalenten Bindung befinden. Wenn dieser Unterschied hoch ist, zieht das hoch elektronegative Atom die Bindungselektronen zu sich selbst an. Dies schafft ein Dipolmoment, in dem dieses hoch elektronegative Atom eine teilweise negative Ladung erhält, während das andere Atom eine teilweise positive Ladung erhält. Dann wird die Bindung zu einer polaren kovalenten Bindung. Wenn dieses Molekül ein anderes Molekül triff. Und diese Anziehungskraft wird als Wasserstoffbindung bezeichnet.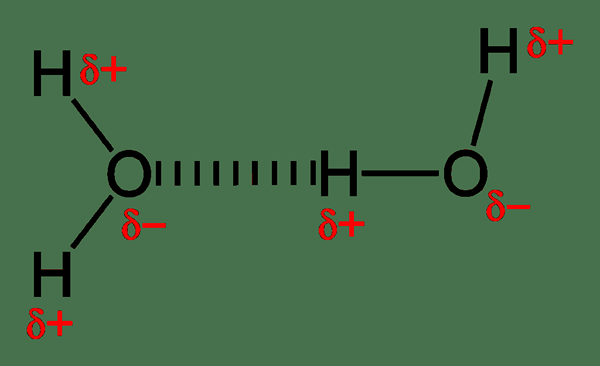
Darüber hinaus werden Wasserstoffbrückenbindungen zwischen hochelektronegativen Atomen und weniger elektronegativen Atomen gebildet. Außerdem existieren sie, wenn wir O, N und F in einem Molekül und positiv geladenem H im anderen Molekül haben. Es liegt daran, dass F, N und O die elektronegativsten Atome sind.
Was ist der Unterschied zwischen Salzbrücken und Wasserstoffbrückenbindung?
Salzbrücke und Wasserstoffbindung sind wichtig für die Hauptverbindung zwischen den gewünschten Objekten. Beispielsweise verbindet eine Salzbrücke zwei halbe Zellen einer elektrochemischen Zelle, während die Wasserstoffbrücke zwei Moleküle verbindet. Der Hauptunterschied zwischen Salzbrücke und Wasserstoffbindung besteht darin, dass eine Salzbrücke ein Röhrchen mit einem Elektrolyt ist, der zwei halbe Zellen in einer elektrochemischen Zelle verbindet. Eine Wasserstoffbindung ist jedoch eine Anziehungskraft zwischen zwei Atomen von zwei verschiedenen Molekülen.
Die folgende Infografik fasst den Unterschied zwischen Salzbrücke und Wasserstoffbrückenbindung zusammen.

Zusammenfassung -Salzbrücke gegen Wasserstoffbrückenbindung
Salzbrücke und Wasserstoffbindung sind wichtig für die Aufrechterhaltung der Konnektivität zwischen den gewünschten Objekten. Beispielsweise verbindet die Salzbrücke zwei halbe Zellen einer elektrochemischen Zelle, während die Wasserstoffbrücke zwei Moleküle verbindet. Der wichtigste Unterschied zwischen Salzbrücke und Wasserstoffbrückenbindung besteht darin.
Referenz:
1. Helmenstine, Anne Marie. „Salzbrückendefinition.”Thoughtco, Jul. 3, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Galvanische Zelle" von Gringer - Datei: Galvanische Zelle.PNG nach Tinux (CC BY-SA 3.0) über Commons Wikimedia
2. "Wasserstoffbrückenbindungen-in-Wasser-2D" (Public Domain) über Commons Wikimedia


