Unterschied zwischen SO2 und SO3
Der Schlüsselunterschied Zwischen SO2 und SO3 ist das SO2 ist ein farbloses Gas bei Raumtemperatur, während dies so ist3 ist eine farblose bis weiße kristalline Feststoff.
SO2 ist Schwefeldioxid während3 ist Schwefeltrioxid. Beide sind Schwefeloxide.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist SO2
3. Was ist SO3
4. Seite an Seite Vergleich - SO2 gegen SO3 in tabellarischer Form
5. Zusammenfassung
Was ist SO2?
SO2 ist Schwefeldioxid. Es ist eine farblose gasförmige Verbindung, die Schwefel- und Sauerstoffatome enthält. SO2 ist die chemische Formel dieser Verbindung. Daher enthält es ein Schwefelatom, das über kovalente Bindungen an zwei Sauerstoffatome gebunden ist. Ein Sauerstoffatom kann eine Doppelbindung zum Schwefelatom bilden. Daher ist das Schwefelatom das zentrale Atom der Verbindung. Das Schwefelatom hat 6 Elektronen im äußersten Orbital. Nachdem zwei Doppelbindungen mit den Sauerstoffatomen gebildet wurden, sind noch zwei weitere Elektronen übrig; Diese Elektronen existieren als einsames Elektronenpaar.
Daher können wir die Geometrie des SO bestimmen2 Molekül; Es ist Winkelgeometrie. SO2 ist polar aufgrund seiner Geometrie (Winkel) und dem Vorhandensein eines einzigen Elektronenpaars.
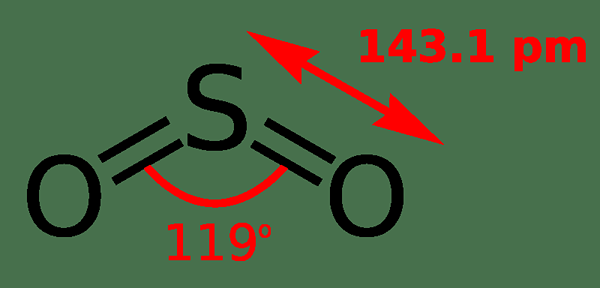
Abbildung 01: Struktur des Schwefeldioxids
Schwefeldioxid wird als giftiges Gas angesehen. Wenn es in der Atmosphäre SO2 gibt, wird dies ein Hinweis auf die Luftverschmutzung sein. Auch dieses Gas hat einen sehr irritierenden Geruch. Die Molekülmasse von Schwefeldioxid beträgt 64 g/mol. Es ist ein farbloses Gas bei Raumtemperatur. Der Schmelzpunkt beträgt etwa -71 ° C, während der Siedepunkt -10 ° C beträgt.
Der Oxidationszustand von Schwefel in Schwefeldioxid beträgt +4. Daher kann Schwefeldioxid auch durch Reduktion von Verbindungen aus Schwefelatomen erzeugt werden, die sich in einem höheren Oxidationszustand befinden. Ein solches Beispiel ist die Reaktion zwischen Kupfer und Schwefelsäure. Hier befindet sich Schwefel in Schwefelsäure im Oxidationszustand von +6. Daher kann es auf den +4 Oxidationszustand von Schwefeldioxid reduziert werden.
Schwefeldioxid kann bei der Herstellung von Schwefelsäure verwendet werden, die eine Reihe von Anwendungen im industriellen Maßstab und in der Laborskala enthält. Schwefeldioxid ist auch ein gutes Reduktionsmittel. Da der Oxidationszustand von Schwefel +4 in Schwefeldioxid beträgt, kann er leicht auf +6 Oxidationszustand oxidiert werden, wodurch eine andere Verbindung reduziert werden kann.
Was ist SO3?
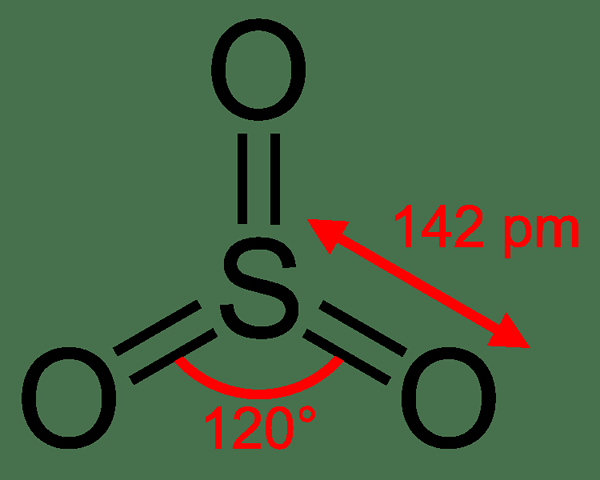
SO3 ist Schwefeltrioxid. Es ist eine feste Verbindung, die ein Schwefelatom enthält, das mit drei Sauerstoffatomen bindet. SO3 ist die chemische Formel dieser Verbindung. Hier hat jedes Sauerstoffatom eine Doppelbindung zum Schwefelatom. Das Schwefelatom befindet sich in der Mitte des Moleküls. Ein Schwefelatom hat 6 Elektronen im äußersten Orbital. Nachdem drei Doppelbindungen mit den Sauerstoffatomen hergestellt wurden. Dies bestimmt die Geometrie des SO3 Molekül; Es hat eine trigonale planare Geometrie. SO3 ist aufgrund seiner Geometrie (trigonaler Planar) und des Fehlens eines einzigen Elektronenpaars nicht Polarisch.

Abbildung 02: Geometrie des Schwefeltrioxids
Die molekulare Masse des Schwefeltrioxids beträgt 80.057 g/mol. Der Schmelzpunkt von so3 ist ungefähr 16.9 ° C, während der Siedepunkt 45 ° C beträgt. Bei Raumtemperatur und Druck ist Schwefeltrioxid eine weiße kristalline feste Verbindung, die in der Luft fäen bleibt. Es hat einen scharfen Geruch. Der Oxidationszustand von Schwefel in Schwefeltrioxid beträgt +6.
In seiner gasförmigen Form ist Schwefeltrioxid ein Luftschadstoff und eine Hauptbestandteil bei sauren Regenfällen. Schwefeltrioxid ist jedoch sehr wichtig für die Produktion von Schwefelsäure im industriellen Maßstab. Es liegt daran, dass Schwefeltrioxid die Anhydridform von Schwefelsäure ist.
SO3 (l) + H2Ö(l) → h2SO4 (l)
Die obige Reaktion ist sehr schnell und exotherm. Daher sollten Kontrollmethoden verwendet werden. Außerdem ist Schwefeltrioxid ein wesentliches Reagenz im Sulfonierungsprozess.
Was ist der Unterschied zwischen SO2 und SO3?
SO2 ist Schwefeldioxid während3 ist Schwefeltrioxid. Beide sind Schwefeloxide. Der Hauptunterschied zwischen SO2 und SO3 ist das so2 ist ein farbloses Gas bei Raumtemperatur, während dies so ist3 ist eine farblose bis weiße kristalline Feststoff. Darüber hinaus beträgt der Oxidationszustand von Schwefel in Schwefeldioxid +4, während es in Schwefeltrioxid +6 beträgt. Aufgrund des Vorhandenseins eines einzigen Elektronenpaares und ihrer Geometrie ist Schwefeldioxid eine polare Verbindung, während Schwefeltrioxid eine unpolare Verbindung ist. Die folgende Infografik fasst den Unterschied zwischen SO2 und SO3 zusammen.

Zusammenfassung -SO2 gegen SO3
SO2 ist Schwefeldioxid und so3 ist Schwefeltrioxid. Beide sind Schwefeloxide. Der Hauptunterschied zwischen SO2 und SO3 ist das so2 ist ein farbloses Gas bei Raumtemperatur, während dies so ist3 ist eine farblose bis weiße kristalline Feststoff.
Referenz:
1. Brandt, Malcolm J., et al. „Chemische Lagerung, Dosierung und Kontrolle.”Tworts Water Supply, 2017, PP. 513-552., doi: 10.1016/B978-0-08-100025-0.00012-0.
Bild mit freundlicher Genehmigung:
1. "Sulfur-Dioxid-2D" vom ursprünglichen Uploader war Richtom80 bei English Wikipedia. - Übertragen von en.Wikipedia to Commons (Public Domain) über Commons Wikimedia
2. "Schwefeltrioxid-2D-Dimensionen" von Jynto-eigene Arbeit, basierend auf der Datei: Schwefeltrioxid-2D-Dimensionen.PNG (Public Domain) über Commons Wikimedia


