Unterschied zwischen quadratischen planaren und tetraedrischen Komplexen
Der Schlüsselunterschied Zwischen quadratischen planar- und tetraedrischen Komplexen ist das Quadratische planare Komplexe haben ein vierstufiges Kristallfelddiagramm, aber die tetraedrischen Komplexe haben ein zweistufiges Kristallfelddiagramm.
Die Kristallfeldtheorie ist eine Theorie in der Chemie, die das Brechen von Elektronenorbitalen (hauptsächlich D- und F -Orbitalen) aufgrund des statischen elektrischen Feldes beschreibt, das durch die anionische Ladung in der Umgebung eines Atoms erzeugt wird. Die Theorie ist sehr wichtig, um die Eigenschaften von Übergangsmetallkomplexen zu beschreiben. Wir können auch die Strukturen von quadratischen planaren und tetraedrischen Komplexen beschreiben.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind quadratische planare Komplexe
3. Was sind tetraedrische Komplexe
4. Seite an Seite Vergleich - quadratischer Planar vs. Tetraedrische Komplexe in tabellarischer Form
5. Zusammenfassung
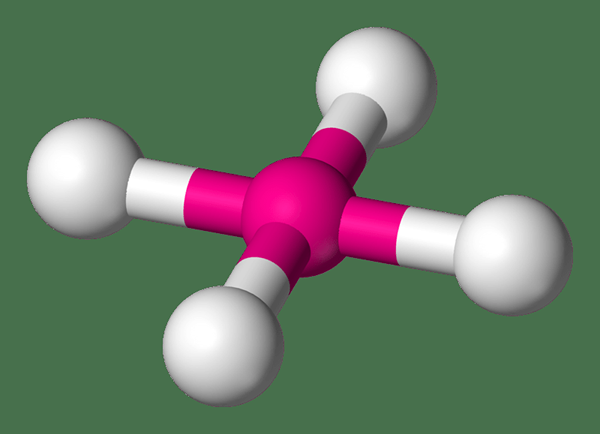
Was sind quadratische planare Komplexe
Quadratische planare Komplexe sind Koordinationskomplexe mit einem zentralen Metallatom, das von vier konstituierenden Atomen in Ecken derselben quadratischen Ebene umgeben ist. Die Bindungswinkel der Bindungen in dieser Struktur betragen 90 °. Übergangsmetalle mit der Elektronenkonfiguration endeten D8 Formen Sie Koordinationskomplexe mit dieser molekularen Geometrie. Zum Beispiel rh (i), ir (i), pd (ii) usw. Die Koordinationsnummer für einen quadratischen planaren Komplex beträgt vier.
Wir können die Struktur dieser Komplexe unter Verwendung der Kristallfeldtheorie (CFT) beschreiben. Nach dieser Theorie hat ein quadratischer planarer Komplex ein vierstufiges Kristallfelddiagramm. Und diese vierstufige Aufteilung heißt D4H. Die resultierenden vier Energieniveaus werden D genanntx2-y2, Dxy, DZ2, und [dxz, Dyz]. Darüber hinaus besteht eine spezifische Beziehung zwischen der quadratischen planaren Geometrie und der tetraedrischen Geometrie. Wir können eine tetraedrische Geometrie in eine quadratische planare Geometrie umwandeln, indem wir das Tetraeder abflachen. Und diese Umwandlung bietet einen Weg zur Isomerisierung der tetraedrischen Komplexe.
Was sind tetraedrische Komplexe?
Tetraedrische Komplexe sind Koordinationskomplexe, die ein zentrales Metallatom haben, das von vier konstituierenden Atomen in Ecken eines Tetraeders umgeben ist. Die Bindungswinkel der Bindungen in dieser Struktur betragen ca. 109.5 °. Wenn sich die Bestandteile jedoch voneinander unterscheiden, variieren die Bindungswinkel. Es gibt zwei Arten von Übergangsmetallen, die diese Art von Komplex bilden können: Metalle mit D0 Konfiguration und d10 Aufbau.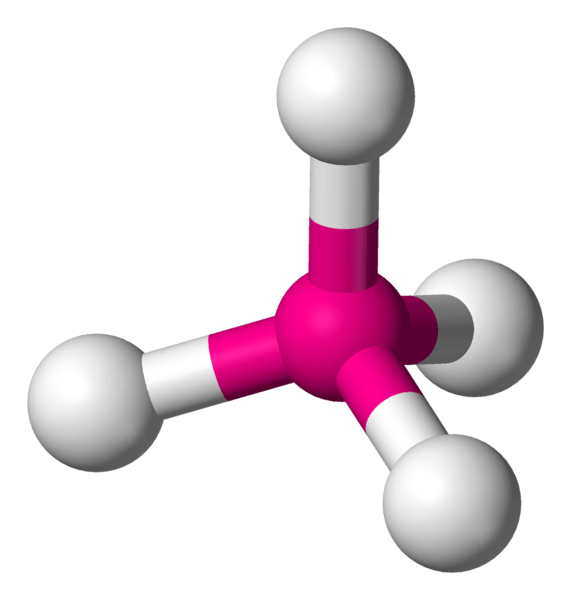
Darüber hinaus haben die tetraedrischen Komplexe nach der Kristallfeldtheorie ein zweistufiges Kristallfelddiagramm. Die beiden Energieniveaus dieses Diagramms umfassen zwei Orbitalssätze: Dxy, Dxz, Dyz in einem Energieniveau und dx2-y2, DZ2 im anderen Satz.
Was ist der Unterschied zwischen quadratischen planaren und tetraedrischen Komplexen?
Die Kristallfeldtheorie ist sehr wichtig für die Beschreibung der Eigenschaften von Übergangsmetallkomplexen sowie die Strukturen von quadratischen planaren und tetraedrischen Komplexen. Der wichtigste Unterschied zwischen quadratischen planaren und tetraedrischen Komplexen besteht darin, dass die quadratischen planaren Komplexe ein vierstufiges Kristallfelddiagramm haben, die tetraedrischen Komplexe jedoch ein zweistufiges Kristallfelddiagramm haben.
Darüber hinaus enden Übergangsmetalle mit ihren Elektronenkonfigurationen mit D8 Die Konfiguration neigt dazu, quadratische planare Komplexe zu bilden, während Metalle mit d0 Konfiguration und d10 Konfiguration bildet tendenziell tetraedrische Komplexe.
Die folgende Infografik zeigt mehr Vergleiche bezüglich des Unterschieds zwischen quadratischen planaren und tetraedrischen Komplexen.
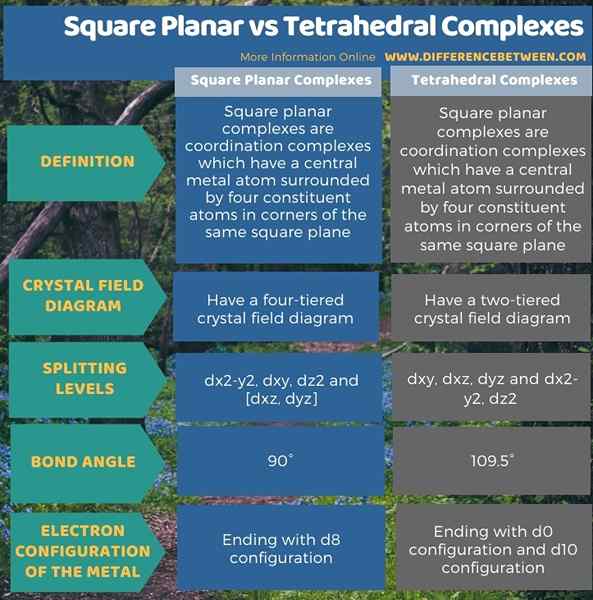
Zusammenfassung -Square Planar vs. Tetraedrische Komplexe
Die Kristallfeldtheorie ist sehr wichtig für die Beschreibung der Eigenschaften von Übergangsmetallkomplexen. Wir können auch die Strukturen von quadratischen planaren und tetraedrischen Komplexen beschreiben. Der wichtigste Unterschied zwischen quadratischen planaren und tetraedrischen Komplexen besteht darin.
Referenz:
1. Mott, Vallerie. „Einführung in die Chemie.”Lumen, hier erhältlich.
2. „Bindung in Koordinationsverbindungen: Kristallfeldtheorie.Grenglose Chemie, Lumen, hier erhältlich.
3. „Kristallfeldtheorie.”Libretexten, hier verfügbar.
Bild mit freundlicher Genehmigung:
1. "Square-Planar-3D-Balls" (Public Domain) über Commons Wikimedia
2. "Tetraedrale 3D-Balls" (öffentlich zugänglich) über Commons Wikimedia


