Unterschied zwischen Dampf und Dampf

Der Schlüsselunterschied Zwischen Dampf und Dampf ist das Dampf ist der gasförmige Wasserzustand, während Dampf der gasförmige Zustand jeder Substanz ist.
Wir verwenden den Begriff „Dampf“ als gebräuchlicher Name, um Wasserdampf speziell zu nennen. Der gasförmige Zustand einer anderen Angelegenheit ist "Dampf". Daher ist die Verwendung des Begriffs der Schlüsselunterschied zwischen Dampf und Dampf. Abgesehen davon gibt es einige weitere Unterschiede zwischen Dampf und Dampf, die wir in diesem Artikel beschreiben werden.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Dampf?
3. Was ist Dampf?
4. Seite an Seite Vergleich - Dampf gegen Dampf in tabellarischer Form
5. Zusammenfassung
Was ist Dampf??
Dampf ist einfach, Wasserdampf. Daher beschreibt der Begriff Dampf den gasförmigen Wasserzustand. Es bildet, wenn Wasser kocht. Das bedeutet, dass der Dampf bei Temperaturen über 100 ° C bei Standarddruck existiert. Normalerweise ist Dampf unsichtbar. Wenn wir uns jedoch auf Nassdampf beziehen, bedeutet dies sichtbarer Nebel oder Aerosol. Der nasse Dampf bildet sich infolge einer Kondensation von Dampf als Wassertröpfchen.

Abbildung 01: Das kochende Wasser erzeugt Dampf
Die Enthalpie der Verdampfung gibt die Energie, die wir benötigen, um Dampf aus Wasser bei Standardtemperatur und Druck zu erzeugen. Wir können diese Änderung der Enthalpie als nützliche Energie verwenden, indem wir mit Dampfmaschinen in mechanische Arbeiten umwandeln.
Nachfolger sind die Verwendung von Dampf;
- In der Landwirtschaft ist es nützlich für die Sterilisation des Bodens, um die Bodengesundheit zu erhöhen.
- In der Küche können wir es zum Dampfkochen von Gemüse verwenden.
- Wir können es für Heizungsgebäude verwenden.
- Nützlich beim Bügeln der Kleidung.
- Etwa 90% der von uns verwendeten Strom werden mit Dampfenergie erzeugt.
- Wir können Dampf unter Druck in Autoklaven verwenden.
Was ist Dampf??
Dampf ist der gasförmige Zustand jeder Substanz. Dieser gasförmige Zustand existiert jedoch bei niedrigeren Temperaturen als die kritische Temperatur dieser Substanz. Daher können wir diesen Dampf in eine flüssige Form kondensieren, indem wir den Druck auf den Dampf erhöhen und gleichzeitig die Temperatur so halten, wie sie ist. Der Dampf unterscheidet sich von Aerosol, da Aerosol winzige Partikel aus flüssigen, festen oder beides in einem Gas enthält.

Abbildung 02: Joddampf hat eine violette Farbe
Der Siedepunkt der Substanz bestimmt die Temperatur, bei der sich der Dampf bildet und existiert. Darüber hinaus kann Dampf mit seiner flüssigen oder festen Phase im Gleichgewicht miteinander existieren. Noch wichtiger ist, dass es nicht wichtig ist, eine Substanz zu kochen, um einen Dampf zu bilden. Einige Substanzen sind flüchtig, was bedeutet, dass diese Substanzen bei normalen Temperatur- und Druckbedingungen in den gasförmigen Zustand verwandeln können. Bei der Betrachtung der Verwendung von Dampf enthalten Parfums eine Substanz, die leicht verdampfen kann, um Dampfdämpfe zu bilden. Wasserdampf kann zusammenarbeiten, um Nebel zu bilden, Quecksilber-Dampf-Lampen können das Licht bilden usw.
Was ist der Unterschied zwischen Dampf und Dampf?
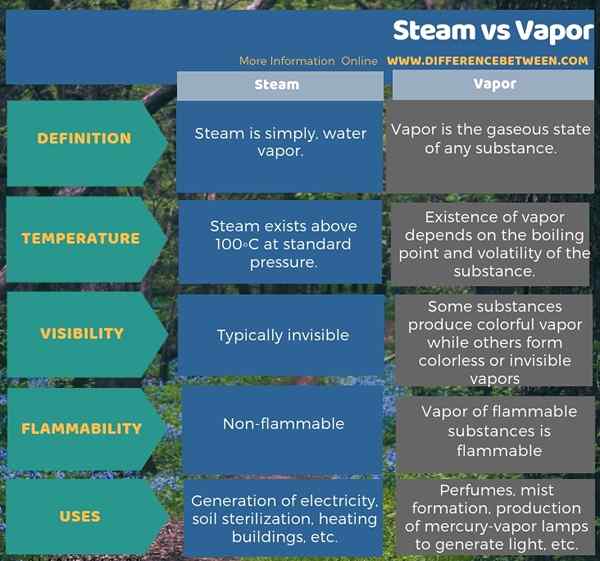
Dampf ist einfach Wasserdampf, während Dampf der gasförmige Zustand jeder Substanz ist. Dies ist daher der Hauptunterschied zwischen Dampf und Dampf. Ein weiterer Unterschied zwischen Dampf und Dampf besteht darin, dass der Dampf bei Standarddruck über 100 ° C liegt, während die Existenz von Dampf vom Siedepunkt und der Volatilität der Substanz abhängt. Wenn wir auch die Sichtbarkeit berücksichtigen, können wir einen Unterschied zwischen Dampf und Dampf identifizieren. Das ist; Der Dampf ist in der Regel unsichtbar, während der Dampf einiger Substanzen farbenfroh ist. Vor allem ist der Dampf aus entflammbaren Substanzen brennbar, aber der Dampf ist nicht entzündlich.
Die folgende Infografik zum Unterschied zwischen Dampf und Dampf tabelt die oben diskutierten Unterschiede auf.
Zusammenfassung -Dampf gegen Dampf
Dampf ist einfach, Wasserdampf. Daher besteht der Hauptunterschied zwischen Dampf und Dampf darin, dass Dampf der gasförmige Wasserzustand ist, während Dampf der gasförmige Zustand einer Substanz ist. Darüber hinaus ist Dampf in der Regel unsichtbar, während der Dampf einiger Substanzen farbenfroh ist.
Referenz:
1. „Was ist der Dampf??”Mel Science. Hier verfügbar
2. "Dampf.Wikipedia, Wikimedia Foundation, 2. Oktober. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Kochendesser02" von Benutzer: Markus Schweiss - eigene Arbeit (CC BY -SA 3).0) über Commons Wikimedia
2."Iodoatomico" von Matias Molnar - Laboratorio Quimica Inorganica II - UBA, Argentinien, (CC BY -SA 3).0) über Commons Wikimedia


