Unterschied zwischen Sublimation und Ablagerung

Der Schlüsselunterschied Zwischen Sublimation und Ablagerung ist das Sublimation ist die Veränderung einer festen Substanz in eine gasförmige Substanz, ohne eine flüssige Phase zu durchlaufen, während Ablagerung die Änderung einer Substanz von einer Gasphase zu einer festen Phase ist, ohne den Flüssigkeitszustand zu übergeben.
Phasenübergang bezieht sich auf die Änderung der Phasen einer Substanz. Externe Faktoren wie Temperatur- und Druckänderungen beeinflussen diesen Prozess. Zum Beispiel verfestigt sich eine Flüssigkeit, wenn wir die Temperatur auf ihren Gefrierpunkt reduzieren, und kann in die Gasphase gehen, wenn sich die Temperatur an ihrem Siedepunkt befindet. Der Phasenübergang hat im Allgemeinen eine Ordnung; Feststoff geht in die flüssige Phase und dann in die Gasphase; oder wenn es sich um ein Gas handelt, sollte es zuerst durch die flüssige Phase und dann in die feste Phase gehen. Sublimation und Ablagerung sind Phasenübergänge, sind jedoch etwas anders als normale Übergänge, da sie dieser Reihenfolge nicht folgen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Sublimation
3. Was ist Ablagerung
4. Seite an Seitenvergleich - Sublimation gegen Abscheidung in tabellarischer Form
5. Zusammenfassung
Was ist Sublimation?
Sublimation ist der Prozess, eine feste Substanz in eine gasförmige Substanz zu verwandeln, ohne die flüssige Phase zu durchlaufen. In einfachen Worten verdunstet eine feste Substanz direkt und wird zu einem Gas, ohne zuerst eine Flüssigkeit zu sein. Dieser Prozess benötigt jedoch zusätzliche Energie. Daher ist dies ein endothermes Prozess. Durch die Berechnung der Entzalpie der Sublimation können wir die für diesen Prozess erforderliche Energie berechnen.
Sublimation tritt bei Temperaturen und Drücken unter dem dreifachen Punkt der Substanz auf. Zum Beispiel bei einer sehr niedrigen Temperatur (-78.5 ° C) und bei atmosphärischem Druck. Der dreifache Punkt des Kohlendioxids beträgt 5.2 atm und -56.4 ° C und darüber können wir auch flüssiges Kohlendioxid erhalten. Eis und Jod können ebenfalls Sublimation erfahren.

Abbildung 1: Sublimation von Trockeneis
Bei Sublimation bleiben die chemischen Eigenschaften der Verbindung unverändert, aber die physikalischen Eigenschaften können sich ändern. Sublimation ist für verschiedene Zwecke nützlich. Zum Beispiel wird es verwendet, um chemische Verbindungen zu reinigen.
Was ist Ablagerung?
Ablagerung ist der entgegengesetzte Prozess der Sublimation. Es ist auch als De-Sublimation bekannt. Hier ändert sich eine Substanz in der Gasphase in die feste Phase, ohne den Zwischenflüssigkeitszustand zu bestehen.

Abbildung 2: Frostbildung
Im Gegensatz zum vorherigen Prozess setzt dieser Prozess Energie frei. Daher ist es ein exothermer Prozess. Darüber hinaus geschieht dies bei der Bildung von Eis oder Frost. In diesem Prozess geht Wasserdampf direkt in die feste Phase (bildet Eis oder Frost). In diesem Fall entfernen sie die thermische Energie in die äußere Umgebung.
Was ist der Unterschied zwischen Sublimation und Ablagerung?
Sublimation ist das Gegenteil von Ablagerung. Der Schlüsselunterschied zwischen Sublimation und Ablagerung besteht darin, dass Sublimation die Änderung einer festen Substanz in eine gasförmige Substanz ist, ohne die flüssige Phase durchzuführen, während die Ablagerung die Änderung einer Substanz von einer Gasphase zu einer festen Phase ist, ohne den Flüssigkeitszustand zu bestehen.
Darüber hinaus besteht ein signifikanter Unterschied zwischen Sublimation und Ablagerung darin, dass Sublimation endotherm ist, während die Ablagerung exotherm ist.
Die folgende Infografik liefert mehr Details zum Unterschied zwischen Sublimation und Ablagerung.
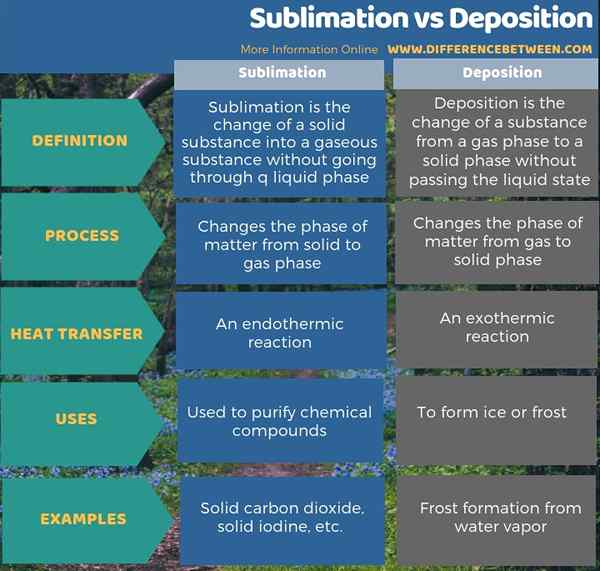
Zusammenfassung -Sublimation gegen Abscheidung
Sublimation ist das Gegenteil von Ablagerung. Beide Prozesse beinhalten jedoch keine flüssige Phase. Der Hauptunterschied zwischen Sublimation und Ablagerung besteht darin, dass Sublimation darin besteht, eine feste Substanz in eine gasförmige Substanz zu verwandeln, ohne die flüssige Phase zu durchlaufen, während die Ablagerung eine Substanz von einer Gasphase zu einer festen Phase ändert, ohne den Flüssigkeitszustand zu bestehen.
Referenz:
1. „Ablagerung (Phasenübergang).Wikipedia, Wikimedia Foundation, 27. März. 2019, hier erhältlich.
2. Helmenstine, Anne Marie, ph.D. „Sublimationsdefinition (Phasenübergang in der Chemie).”Thoughtco, Jan. 13, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Dryicesublimation" von Sarathtly - Foto von mir (öffentlich zug) über Commons Wikimedia aufgenommen
2. "Frost Muster 4" von Schnobby - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia


