Unterschied zwischen Valenz und Valenzelektronen
Schlüsselunterschiede - Valenz gegen Valenzelektronen
Valenzelektronen und Valenzelektronen sind miteinander verbundene Begriffe und die Schlüsselunterschied zwischen Valenz und Valenzelektronen wird am besten in ihren Definitionen erklärt; Valenzelektronen sind die Elektronen in der äußersten Hülle eines Elements wohingegen Valenzelektronen sind die Anzahl der Elektronen, die akzeptiert oder entfernt werden sollten, um die nächste Edelgaskonfiguration zu erreichen. Es sind die Elektronen in der äußersten Hülle, die normalerweise dazu beitragen, chemische Bindungen zu bilden. In einigen Atomen entspricht die Anzahl der Valenzelektronen der Anzahl der Valenzelektronen.
Was sind vALENCE -Elektronen?
Die Anzahl der Elektronen in der äußersten Hülle eines Atoms wird als „Valenzelektronen“ bezeichnet. Aus diesem Grund wird die äußerste Hülle eines Atoms als „Valenzschale“ bezeichnet. Meistens sind dies die Elektronen, die an einer chemischen Bindung teilnehmen. Wenn Elemente Kationen bilden, entfernen sie Elektronen aus der Valenzschale. Die Anzahl der Valenzelektronen in einem Element bestimmt die Gruppe in der Periodenzüchtertabelle.
Was sind Valenzelektronen?
Die Anzahl der Elektronen, die erforderlich sind, um die äußerste Hülle eines Atoms zu gewinnen oder zu verlieren, wird als „Valenzelektronen“ bezeichnet. Für ein bestimmtes Atom hängt die Anzahl der Valenzelektronen von der Anzahl der Valenzelektronen im Atom ab. Für Natrium beträgt die Valenz 1, da es das letzte Elektron in der äußersten Schale entfernt, um die Oktettstruktur des nächsten Edelgas zu erreichen.
|
Was ist der Unterschied zwischen Valenz und Valenzelektronen?
Definition von Valenz- und Valenzelektronen
Valenzelektronen: Die Elektronen in der äußersten Schale eines Atoms werden als „Valenzelektronen“ bezeichnet. Für "S" und "P" -Gruppenelemente entspricht die Anzahl der Valenzelektronen ihrer Gruppenzahl.
Beispiel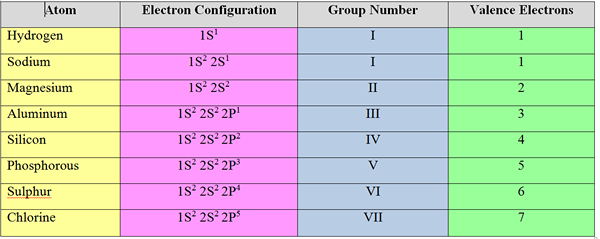
Valenzelektronen: Die Anzahl der Elektronen, die akzeptiert oder entfernt werden sollten, um die Elektronenkonfiguration des nächsten Edelgas zu erreichen.
Im Allgemeinen ist die Anzahl der Valenzelektronen für Metallelemente (Elemente in Gruppe I, II und III) gleich der Anzahl der Valenzelektronen; Sie entfernen die Elektronen in der Valenzschale, um die Oktettstruktur zu erreichen.
Nichtmetallelemente akzeptieren jedoch Elektronen, um die Elektronenkonfiguration des nächsten Edelgas zu erreichen. Daher wird die Valenz nicht-metaler Elemente berechnet, indem die Gesamtvalenzelektronen von 8 subtrahiert werden.
Für Chlor, Anzahl der Valenzelektronen = 8-7 = 1
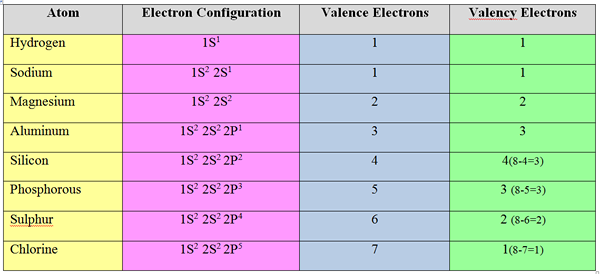
Eigenschaften von Valenz- und Valenzelektronen
Valenz- und Valenzelektronen der Elemente der Gruppe VIII
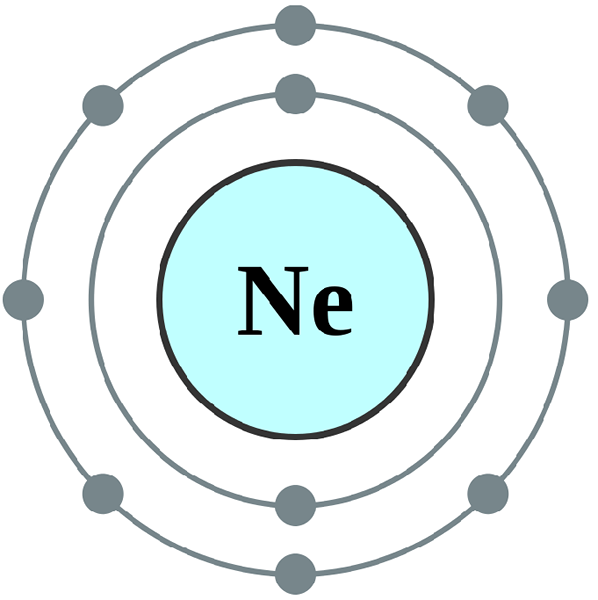
Valenzelektronen: Elemente der Gruppe VIII sind die edlen Gase und sie sind chemisch stabil. Ihre äußere Hülle ist vollständig und enthält acht Elektronen in der äußersten Hülle (außer Helium -He); Damit die Gruppe VIII -Elektronen acht Valenzelektronen haben.
Valenzelektronen: Valenz ist ein Maß für die Fähigkeit, Bindungen mit anderen Elementen oder Molekülen zu formen. Edelgase akzeptieren oder entfernen keine Elektronen, um die Oktettregel zu erreichen, da sie bereits die letzte Schale abgeschlossen haben. Daher ist die Valenz der Elemente der Gruppe VII gleich Null.
Bild mit freundlicher Genehmigung:
"Electron Shell 010 Neon - kein Etikett" von Commons: Benutzer: Pumbaa (Originalarbeit von Commons: Benutzer: Greg Robson) - http: // Commons.Wikimedia.org/wiki/kategorie: Electron_shell_diagrams (entsprechende beschriftete Version).(CC BY-SA 2.0 uk) über Commons

