Was ist der Unterschied zwischen Ammoniumnitrat und Ammoniumsulfat
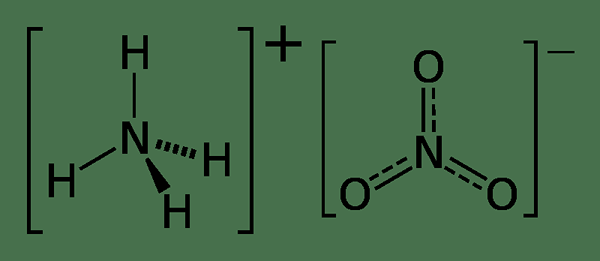
Der Schlüsselunterschied zwischen Ammoniumnitrat und Ammoniumsulfat ist, dass sich Ammoniumnitrat aus der Reaktion zwischen Ammoniak und Salpetersäure bildet, während sich Ammoniumsulfat aus der Reaktion zwischen Ammoniak und Schwefelsäure bildet.
Ammoniumnitrat ist eine anorganische Verbindung mit der chemischen Formel NH4NO3, und Ammoniumsulfat ist eine anorganische Verbindung mit der chemischen Formel (NH4) 2SO4. Beide sind Ammoniaksalze mit einem starken, irritierenden Geruch.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Ammoniumnitrat
3. Was ist Ammoniumsulfat
4. Ammoniumnitrat gegen Ammoniumsulfat in tabellarischer Form
5. Zusammenfassung -Ammoniumnitrat gegen Ammoniumsulfat
Was ist Ammoniumnitrat?
Ammoniumnitrat ist eine anorganische Verbindung mit der chemischen Formel NH4NO3. Diese Substanz ist ein Salz, das aus einem Ammoniumkation und einem Nitratanion besteht. Darüber hinaus erscheint es bei Raumtemperatur als weißer Feststoff und kann sich leicht in Wasser auflösen. Darüber hinaus tritt Ammoniumnitrat als natürlicher mineralischer Natur auf.
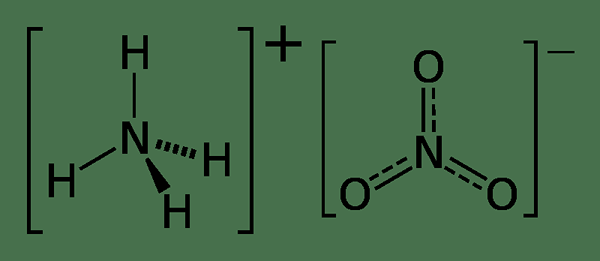
Abbildung 01: Die chemische Struktur von Ammoniumnitrat
Einige chemische Fakten über diese Verbindung sind wie folgt:
- Molmasse ist 80.043 g/mol
- Erscheint als weißer oder grauer Feststoff
- Schmelzpunkt ist 169.6 ° C
- Über 210 ° C zersetzt es sich
- Die Kristallstruktur der Verbindung ist trigonal
Die Hauptverwendung der Ammoniumnitratverbindung findet sich in der Landwirtschaft; Es ist sehr nützlich als Dünger mit hohem Stickstoff. Abgesehen davon können wir es verwenden, um Sprengmischungen für Bergbau- und Steinbruchzwecke zu produzieren. Da die Auflösung dieser Verbindung in Wasser sehr endotherm ist, ist sie auch in einigen sofortigen kalten Packungen nützlich.
Was ist Ammoniumsulfat?
Ammoniumsulfat ist eine anorganische Verbindung mit der chemischen Formel (NH4) 2SO4. Es besteht normalerweise aus einem Ammoniumkation, das mit einem Sulfatanion verbunden ist. Daher hat diese Verbindung zwei Ammoniumkationen pro Sulfatanion. Es ist ein anorganisches Sulfatsalz mit vielen wichtigen Verwendungen.
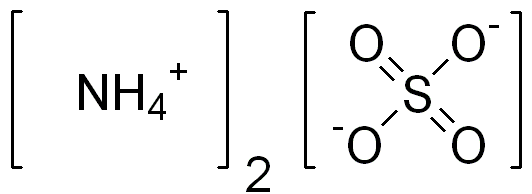
Abbildung 02: Die chemische Struktur von Ammoniumsulfat
Die Molmasse von Ammoniumsulfat beträgt 132.14 g/mol. Diese Verbindung erscheint als feines, hygroskopisches Granulat oder Kristalle. Darüber hinaus kann der Schmelzpunkt dieser Verbindung zwischen 235 und 280 ° C reichen; Über diesem Temperaturbereich zersetzt sich die Verbindung. Wir können Ammoniumsulfatverbindungen produzieren, indem wir Ammoniak mit Schwefelsäure behandeln. Für diese Zubereitung können wir eine Mischung aus Ammoniakgas und Wasserdampf in einem Reaktor verwenden. Darüber hinaus müssen wir in diesem Reaktor konzentrierte Schwefelsäure einfügen, und dann bildet die Reaktion zwischen diesen Komponenten Ammoniumsulfat.
Bei der Betrachtung der Anwendungen von Ammoniumsulfat können wir es als Dünger verwenden, hauptsächlich für alkalische Böden. Darüber hinaus können wir es bei der Herstellung von Insektiziden, Herbiziden, Fungiziden usw. verwenden. Zusätzlich zu diesen verwenden wir diese Verbindung zur Reinigung von Protein durch Niederschlag im Biochemie -Labor. Es ist auch als Lebensmittelzusatz nützlich.
Was ist der Unterschied zwischen Ammoniumnitrat und Ammoniumsulfat?
Ammoniumnitrat und Ammoniumsulfat sind Ammoniumsalze. Der Schlüsselunterschied zwischen Ammoniumnitrat und Ammoniumsulfat besteht darin, dass sich Ammoniumnitrat aus der Reaktion zwischen Ammoniak und Salpetersäure bildet. Darüber hinaus ist Ammoniumnitrat als weißer Kristallfest erhältlich, während Ammoniumsulfat als feines Pulver, Granulat oder Kristalle erhältlich ist, die hygroskopisch sind.
Die folgende Infografik zeigt die Unterschiede zwischen Ammoniumnitrat und Ammoniumsulfat in tabellarischer Form für Seite für Seitenvergleich.
Zusammenfassung -Ammoniumnitrat gegen Ammoniumsulfat
Ammoniumnitrat ist eine anorganische Verbindung mit der chemischen Formel NH4NO3, während Ammoniumsulfat eine anorganische Verbindung mit der chemischen Formel (NH4) 2SO4 ist. Der Schlüsselunterschied zwischen Ammoniumnitrat und Ammoniumsulfat besteht darin, dass sich Ammoniumnitrat aus der Reaktion zwischen Ammoniak und Salpetersäure bildet.
Referenz:
1. "Ammoniumnitrat.” Nationales Zentrum für Biotechnologie Information. Pubchem Compound -Datenbank, U.S. Nationalbibliothek für Medizin.
Bild mit freundlicher Genehmigung:
1. "Ammonium-nitrat-2D" von Mikayé-eigene Arbeit basiert auf: Ammonium-nitrat-2D.PNG (Public Domain) über Commons Wikimedia
2. "Ammoniumsulfat" von Edgar181 - eigene Arbeit (Public Domain) über Commons Wikimedia


