Was ist der Unterschied zwischen Manganoxid und Mangandioxid
Der Schlüsselunterschied zwischen Manganoxid und Mangandioxid ist, dass Manganoxid als grüne Kristalle erscheint, während Mangandioxid als braun oder schwarz fest erscheint.
Manganoxid und Mangandioxid sind anorganische Oxidverbindungen mit Manganatomen, die an Sauerstoffatomen gebunden sind. Beide Verbindungen haben unterschiedliche wichtige Anwendungen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Manganoxid
3. Was ist Mangandioxid
4. Manganoxid gegen Mangan -Dioxid in tabellarischer Form
5. Zusammenfassung -Manganoxid gegen Mangan -Dioxid
Was ist Manganoxid?
Manganoxid ist eine chemische Verbindung mit der chemischen Formel MNO. Wir können diesen Begriff jedoch verwenden, um auf Oxid oder Hydroxid von Mangan zu verweisen, einschließlich Mangan (II) Oxid, Mangan (II, III) Oxid, Mangandioxid und Mangan (vi) Oxid.

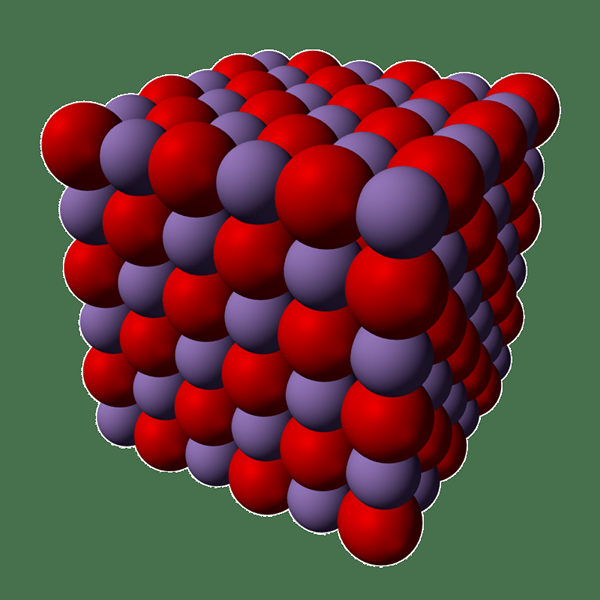
Abbildung 01: Manganoxid
Manganoxid erscheint als grüne Kristalle und wird in großem Maßstab hergestellt, um als Bestandteil in Düngemitteln und Lebensmittelzusatzstücken zu verwendet. Ähnlich wie bei anderen Monoxiden nimmt MNO auch die Steinsalzstruktur an, die im obigen Bild angegeben ist. Es hat Kationen und Anionen, beide oktaedrally koordiniert. Ähnlich wie bei vielen Oxiden ist MNO häufig nicht zur Verfügung1.045).
Die Molmasse des Mangansoxids beträgt 70.93 g/mol. Es hat eine Dichte von ungefähr 5.43 g/mol. Der Schmelzpunkt ist 1945 Grad Celsius und ist in Wasser unlöslich. MNO ist jedoch löslich in Säuren. Die Kristallstruktur dieser Verbindung kann als Halitstruktur beschrieben werden.
Was ist Mangandioxid?
Mangandioxid ist eine anorganische Verbindung mit der chemischen Formel Mno2. Es erscheint als schwarzbrauner fester Substanz und tritt natürlich als Mineralpyrolusit auf. Es ist das Haupterz von Mangan und tritt auch als Bestandteil von Manganknoten vor.

Abbildung 02: Mangandioxid
Die Molmasse des Mangansdioxids beträgt 86.93 g/mol, und die Dichte ist 5.026 g/cm3. Der Schmelzpunkt beträgt ca. 535 Grad Celsius, und bei höheren Temperaturen neigt er dazu, sich zu zersetzen. Es ist jedoch in Wasser unlöslich. Die Kristallstruktur von Mangandioxid ist tetragonal.
Es gibt mehrere Polymorphe von MnO2 sowie eine hydratisierte Form. Ähnlich wie bei vielen anderen Dioxiden kristallisiert diese Substanz in der Rutil -Kristallstruktur, die 3 Koordinatenoxid- und oktaedrische Metallzentren haben. Diese Substanz ist charakteristisch nicht zur Verfügung. Darüber hinaus brauchen wir bei organischen Synthesereaktionen diese Substanz in einem frisch vorbereiteten Zustand. Die Kristallstruktur dieser Verbindung hat eine sehr offene Struktur, die aus Kanälen besteht, die Metallatome aufnehmen, einschließlich Silber und Barium.
Was ist der Unterschied zwischen Manganoxid und Mangandioxid?
Manganoxid und Mangan -Dioxid sind wichtige anorganische Verbindungen, die aus der Oxidation von Manganchemieelementen gebildet werden. Der Hauptunterschied zwischen Manganoxid und Mangandioxid besteht darin. In Manganoxid beträgt der Oxidationszustand von Mangan +2. Darüber hinaus hat Manganoxid eine tetragonale Kristallstruktur, während Mangandioxid eine Halitkristallstruktur hat.
Die folgende Infografik stellt die Unterschiede zwischen Manganoxid und Mangandioxid in tabellarischer Form für den Nebenseitigen Vergleich vor.
Zusammenfassung -Manganoxid gegen Mangan -Dioxid
Manganoxid und Mangandioxid sind Oxide von Manganer. Der Begriff Manganoxid wird jedoch manchmal als kollektiver Name verwendet, um sich auf alle Oxide und Hydroxide zu beziehen, die von manganchemischen Elementen hergestellt wurden. Der Hauptunterschied zwischen Manganoxid und Mangandioxid besteht darin.
Referenz:
1. „Manganoxid.” Ein Überblick | Sciencedirect -Themen.
Bild mit freundlicher Genehmigung:
1. "Mangan (ii) -oxid-textal-3d-sf" von CCOIL (DECK)-eigene Arbeit (CC BY-SA 3.0) über Commons Wikimedia
2. "Mangan (iv) Oxid" von Walkerma Angenommen - keine maschinenlesbare Quelle zur Verfügung gestellt. Eigene Arbeit angenommen (basierend auf Urheberrechtsansprüchen). (Public Domain) über Commons Wikimedia


