Was ist der Unterschied zwischen der molekularen Geometrie und der Elektronengeometrie
Der Schlüsselunterschied zwischen molekularer Geometrie und Elektronengeometrie ist, dass die molekulare Geometrie durch die kovalenten Bindungen des Moleküls bestimmt wird, während die Elektronengeometrie durch die Elektronenpaare bestimmt wird, die das zentrale Atom eines Moleküls umgeben.
Molekulare Geometrie und Elektronengeometrie sind wichtige Begriffe in der allgemeinen Chemie und machen die Grundlage für die Bestimmung der Eigenschaften chemischer Verbindungen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist molekulare Geometrie
3. Was ist Elektronengeometrie
4. Molekulare Geometrie und Elektronengeometrie in tabellarischer Form
5. Zusammenfassung -Molekulare Geometrie gegen Elektronengeometrie
Was ist molekulare Geometrie?
Die molekulare Geometrie ist die molekulare Struktur einer Verbindung, die in der 3D -Anordnung von Atomen gegeben ist. Mit anderen Worten, es ist die 3D -Strukturanordnung der Atome in einem bestimmten Molekül. Das Studium und Identifizieren dieser räumlichen Anordnung von Atomen kann uns helfen, die Polarität der Verbindung, Reaktivität, Phase der Materie, Farbe, Magnetismus und biologische Aktivität zu bestimmen.
Die molekulare Geometrie zeigt die Form des Moleküls, der Bindung, der Längen, der Bindungswinkel, der Torsionswinkel und anderer geometrischer Parameter, die die Position jedes Atoms bestimmen können. Typischerweise hängen die Bindungswinkel zwischen Atomen nur schwach vom Rest des Moleküls ab.
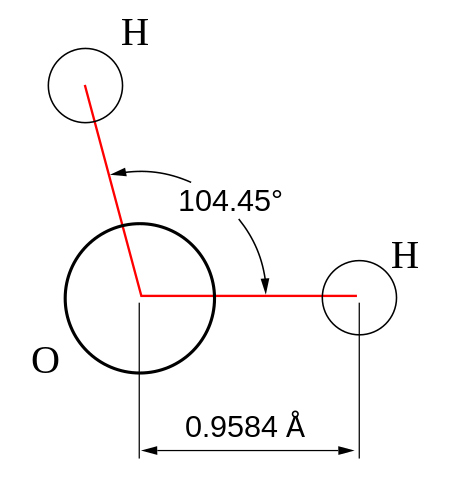
Abbildung 01: Wassermolekül
Es gibt verschiedene Methoden zur Bestimmung der molekularen Geometrie, einschließlich spektroskopischer Methoden wie Beugungsmethoden, IR, Mikrowellen und Raman -Spektroskopie. Diese Methoden können uns Details zur molekularen Geometrie unter Verwendung von Schwingungs- und Rotationsabsorption liefern, die durch die spektroskopische Technik nachgewiesen werden. Darüber hinaus können wir die molekulare Geometrie von kristallinen Festkörpern unter Verwendung von Röntgenkristallographie, Neutronenbeugung und Elektronenbeugung erhalten. Diese Bestimmung erfolgt basierend auf dem Abstand zwischen Kernen und der Konzentration der Elektronendichte. Darüber hinaus kann die Position von Atomen im Molekül durch die Art der chemischen Bindungen bestimmt werden, durch die es mit den benachbarten Atomen verbunden ist.
Was ist Elektronengeometrie?
Elektronengeometrie ist die Anordnung von Elektronenpaaren um ein zentrales Atom. Mit anderen Worten, die Elektronengeometrie ist die 3D-Struktur von Elektronenpaaren (entweder Bindungs- oder nicht gebundene Elektronenpaare) um ein zentrales Atom. Normalerweise ist ein einsames Elektronenpaar oder ein nicht gebundenes Elektronenpaar ein Paar Valenzelektronen, die nicht zwischen Atomen in einer kovalenten Bindung geteilt werden. Ein Bindungselektronenpaar kann als ein Elektronenpaar beschrieben werden, das an einer chemischen Bindung teilnimmt.
Da Elektronen negativ aufgeladen sind, werden Elektronenpaare um ein zentrales Atom voneinander abgestoßen, so. Daher nehmen die Bindungswinkel entsprechend geringfügig ab.

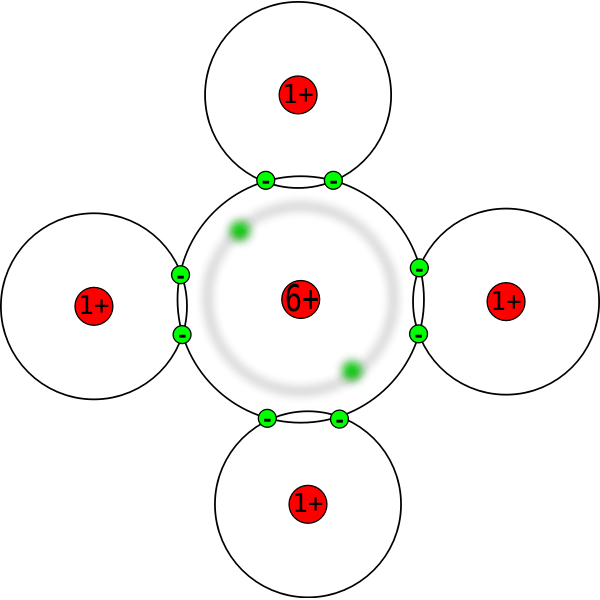
Abbildung 02: Elektronenpaare um das Kohlenstoffatom in einem Methanmolekül um das Kohlenstoffatom.
Wenn alle Elektronenpaare um ein Atom Bindelektronenpaare sind, ist die molekulare Geometrie und die Elektronengeometrie um dieses Atom gleich. Zum Beispiel hat ein Methanmolekül vier Bindungen um das zentrale Kohlenstoffatom, und alle Elektronen um es sind Bindungselektronen. Daher ist die molekulare Geometrie und die Elektronengeometrie dieses Moleküls tetraedrisch.
Was ist der Unterschied zwischen der molekularen Geometrie und der Elektronengeometrie?
Molekulare Geometrie und Elektronengeometrie sind wichtige Begriffe in grundlegenden chemischen Prinzipien und erklären die Bestimmung der chemischen Eigenschaften von Molekülen. Die molekulare Geometrie ist die molekulare Struktur einer Verbindung, die in der 3D -Anordnung von Atomen gegeben ist, während die Elektronengeometrie als Anordnung von Elektronenpaaren um ein zentrales Atom definiert werden kann. Der Schlüsselunterschied zwischen molekularer Geometrie und Elektronengeometrie besteht darin, dass die molekulare Geometrie durch die kovalenten Bindungen des Moleküls bestimmt wird.
Zusammenfassung -Molekulare Geometrie gegen Elektronengeometrie
Molekulare Geometrie und Elektronengeometrie bestimmen die Eigenschaften einer chemischen Verbindung. Der Schlüsselunterschied zwischen molekularer Geometrie und Elektronengeometrie besteht darin, dass die molekulare Geometrie durch die kovalenten Bindungen des Moleküls bestimmt wird.
Referenz:
1. „Geometrie von Molekülen.” Chemie -Libretexten, Libretexten.
Bild mit freundlicher Genehmigung:
1. "Wassermoleküleabmessungen" von Booyabazooka - Bild: Water_Molecule_Dimensions.PNG (CC BY-SA 3.0) über Commons Wikimedia
2. "Atombindung von Methan" (CC0) über freies SVG


