Unterschied zwischen Ascorbinsäure und L-Ascorbinsäure

Ascorbinsäure gegen L-Ascorbinsäure
Ascorbinsäure ist eine organische Verbindung, die als Säure wirken kann. Organische Säuren enthalten im Wesentlichen Wasserstoff und Kohlenstoff mit einem anderen Element/s. Andere Arten der häufigsten organischen Säuren sind Essigsäure, Milchsäure, Ameisensäure, Zitronensäure usw. Diese Säuren haben eine -kooh -Gruppe. Daher können sie als Protonenspender fungieren. Ascorbinsäure ist in Zitrusfrüchten vorhanden. Zum Beispiel können Limette, Zitrone und Orangen als Zitrusfrüchte angesehen werden.
Askorbinsäure
Ascorbinsäure ist auch eine natürlich vorkommende organische Säure. Es ist beim Menschen, Pflanzen und Mikroorganismen vorhanden. Es hat die molekulare Formel von C6H8Ö6. Dies ist eine weiße Farbe fest, kann aber manchmal auch in einer leichten gelben Farbe auftreten. Die gelbliche Farbe repräsentiert den niedrigen Reinheit von Ascorbinsäure. Ascorbinsäure hat die folgende zyklische Struktur mit sauren Gruppen.
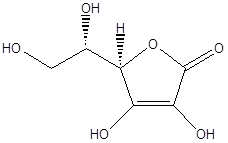
Ascorbinsäure ist in Wasser und anderen polaren organischen Lösungsmitteln löslich. Wenn es in Wasser gelöst ist, bildet es eine milde saure Lösung. Wenn lose Proton aus einer Hydroxylgruppe an Vinylkohlenstoff gebunden ist, wird das Molekül durch Resonanzstabilisierung stabilisiert. Diese Stabilität einer deprotonierten konjugierten Base von Ascorbinsäure macht es saurer als die anderen Hydroxylgruppen. Ascorbinsäure ist ein Antioxidans wie Zitronensäure. Daher reagiert es mit den Oxidationsmitteln der reaktiven Sauerstoffspezies, um schädliche Spezies zu ergeben. Wenn beispielsweise Ascorbinsäure mit Wasserstoffperoxid reagiert, bildet es Hydroxylradikale, die die wichtigen Moleküle in den Zellen beschädigen können. Ascorbinsäure ist ein Reduktionsmittel. Wenn es Luft ausgesetzt ist, reduziert es den Sauerstoff auf Wasser. Wenn Licht- und Metallionen vorhanden sind, beschleunigen diese reduzierenden Reaktionen. In der Synthese von Ascorbinsäure wird Glukose zum Reaktant. Die meisten Tiere können Ascorbinsäuren in ihrem Körper synthetisieren. Die Umwandlung von Glucose zu Ascorbinsäure findet in der Leber statt, und dafür ist das Enzym L-Gulonolactonoxidase erforderlich. Aber einige Tiere wie Fledermäuse, Primaten, Meerschweinchen und Vögel können aufgrund des Fehlens dieses Enzyms keine Ascorbinsäure synthetisieren. Für den Menschen ist dies auch der Fall. Sie sollten also die Ascorbinsäure -Anforderung aus ihrer Ernährung erfüllen.
L-Ascorbinsäure
L-Ascorbinsäure ist auch als Vitamin C bekannt, und dies ist ein wesentlicher Nährstoff für den Menschen. Dies ist die Form von Ascorbinsäure, die Tiere und Menschen in den Körper einnehmen sollten, wenn sie Ascorbinsäure nicht synthetisieren können. Dies ist das L-Enantiomer der Ascorbinsäure und das D-Enantiomer spielt in biologischen Systemen keine signifikante Rolle. Wie oben erwähnt, ist dies die Verbindung, die als Reduktionsmittel und Antioxidans in biologischen Systemen wirkt. Sie sind wichtig für die Synthese von Kollagen, Carnitin, Neurotransmitter, Tyrosin usw. Darüber hinaus wird es als Cofaktor für einen Teil des Syntheseprozesses benötigt. Das Fehlen von Vitamin C führt dazu, dass die Krankheit als Skorbut bezeichnet wird. Symptome dieser Krankheit sind braune Flecken auf der Haut, schwammiges Zahnfleisch und Blutungen durch Schleimhäutemembranen.
| Was ist der Unterschied zwischen Ascorbinsäure und L-Ascorbinsäure? • L -Ascorbinsäure sind die L -Enantiomere von Ascorbinsäure. • L -Ascorbinsäure ist die in biologische Systeme reichlich vorhandene Verbindung als die D -Ascorbinsäure. • Einige Organismen können L-Ascorbinsäure in ihrem Körper synthetisieren. |


