Unterschied zwischen Benzoesäure und Ethylbenzoat
Der Schlüsselunterschied Zwischen Benzoesäure und Ethylbenzoat ist das die Benzoesäure enthält einen Benzolring, der an einer Carboxsäuregruppe gebunden ist, während das Ethylbenzoat einen Benzolring enthält, der an einer Estergruppe angebracht ist.
Benzoesäure ist eine aromatische Carboxylsäure, während Ethylbenzoat ein aromatischer Ester ist. Da es sich um aromatische Verbindungen handelt, haben beide Verbindungen einen süßen und angenehmen Geruch.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Benzoesäure
3. Was ist Ethylbenzoat
4. Seite an Seitenvergleich - Benzoesäure gegen Ethylbenzoat in tabellarischer Form
5. Zusammenfassung
Was ist Benzoesäure?
Benzoesäure ist eine Carbonsäure mit der chemischen Formel C7H6Ö2. Es ist die einfachste aromatische Carboxylsäure und tritt als farbloser kristalline Feststoff auf. Außerdem tritt diese Verbindung natürlich in vielen Pflanzen auf, weil sie als Zwischenprodukt bei der Herstellung von sekundären Metaboliten wirkt.
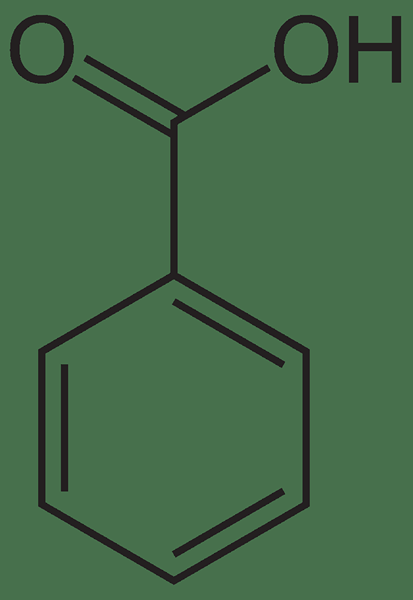
Abbildung 01: Chemische Struktur von Benzoesäure
Darüber hinaus ist die Molmasse 122.12 g/mol. Es hat einen angenehmen Geruch. Sein Schmelzpunkt beträgt 122 ° C, während der Siedepunkt 250 ° C beträgt. Für den industriellen Bedarf können wir dieses Material durch teilweise Oxidation von Toluol in Gegenwart von Sauerstoff produzieren. Darüber hinaus stammt der Name dieser Verbindung aus ihrer Struktur, die einen Benzolring mit einer angeschlossenen Carboxylsäuregruppe hat.
Bei der Betrachtung der Verwendung von Benzoesäure ist es für die Herstellung von Phenol als Vorläufer für die Herstellung von Weichmachern, als Vorläufer für die Herstellung von Natriumbenzoat, ein nützlicher Konservierungsmittel für Lebensmittel usw.
Was ist Ethylbenzoat?
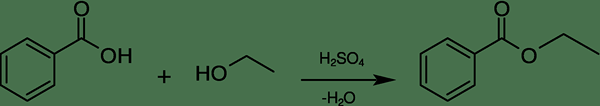
Ethylbenzoat ist ein aromatischer Ester mit der chemischen Formel C9H10Ö2. Die Verbindung bildet sich aus der Kondensation von Benzoesäure und Ethanol. Es tritt als farblose Flüssigkeit auf, die einen süßen, wintergrünen Geruch hat. Die Molmasse beträgt 150.177 g/mol. Sein Schmelzpunkt beträgt –34 ° C, während der Siedepunkt von 211 bis 213 ° C reicht.

Abbildung 02: Herstellung von Ethylbenzoat
Darüber hinaus ist diese Verbindung in Wasser fast unlöslich, löst sich jedoch in organischen Lösungsmitteln auf. Aufgrund seines süßen Geruchs wird diese Verbindung als Bestandteil in Duftstoffe und als künstliche Fruchtbevorzugungen verwendet. Die häufigste Methode zur Herstellung von Ethylbenzoat ist die saure Veresterung von Benzoesäure mit Ethanol in Gegenwart von Schwefelsäure als Katalysator.
Was ist der Unterschied zwischen Benzoesäure und Ethylbenzoat?
Benzoesäure ist eine Carbonsäure mit der chemischen Formel C7H6Ö2 Während Ethylbenzoat ein aromatischer Ester mit der chemischen Formel C ist9H10Ö2. Der wichtigste Unterschied zwischen Benzoesäure und Ethylbenzoat besteht darin, dass die Benzoesäure einen Benzolring enthält, der an einer Carboxylsäuregruppe gebunden ist, während das Ethylbenzoat einen Benzolring enthält, der an einer Estergruppe gebunden ist.
Darüber hinaus können wir auch einen Unterschied zwischen Benzoesäure und Ethylbenzoat erkennen, die auf ihren physikalischen Eigenschaften basieren. Die Benzoesäure tritt als farbloser kristalliner Feststoff auf, während das Ethylbenzoat als farblose Flüssigkeit auftritt. Wenn Sie den Geruch dieser Verbindungen berücksichtigen, hat Benzoesäure einen schwachen und angenehmen Geruch, während Ethylbenzoat einen süßen, wintergrünen Geruch hat. Außerdem ist Benzoesäure schlecht wasserlöslich, aber Ethylbenzoat ist in Wasser fast unlöslich und in den meisten organischen Lösungsmitteln löslich.
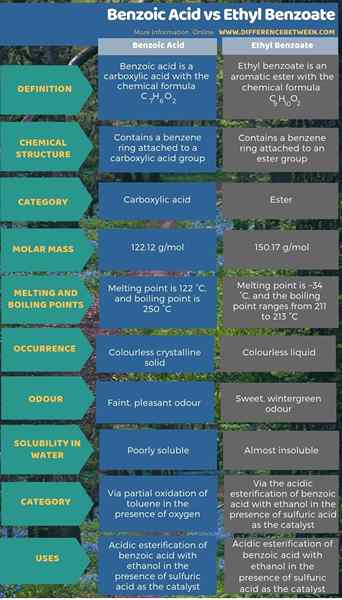
Zusammenfassung -Benzoesäure gegen Ethylbenzoat
Benzoesäure ist eine Carbonsäure mit der chemischen Formel C7H6Ö2 Während Ethylbenzoat ein aromatischer Ester ist, der die chemische Formel C hat9H10Ö2. Vor allem der Hauptunterschied zwischen Benzoesäure und Ethylbenzoat besteht darin.
Referenz:
1. "Benzoesäure.Nationales Zentrum für Biotechnologieinformationen. Pubchem Compound -Datenbank, u.S. National Library of Medicine, hier verfügbar.
Bild mit freundlicher Genehmigung:
1. "Benzoesäure" von Neurotiker - eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Ethyl Benzoat -Veresterung" von Minihaa - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia


