Unterschied zwischen Carbonyl- und Nitrosylkomplexen
Der Schlüsselunterschied zwischen Carbonyl- und Nitrosylkomplexen ist, dass Carbonylkomplexe -co -Liganden enthalten, während Nitrosylkomplexe -no -Liganden enthalten.
Koordinationskomplexe sind anorganische Komplexe, die ein zentrales Atom oder ein Ion (typischerweise ein Metallion) und umgebende Moleküle namens Liganden enthalten, die an das zentrale Atom oder Ion gebunden sind. Das zentrale Atom oder Ion wird normalerweise als Koordinierungszentrum bezeichnet.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind Carbonylkomplexe
3. Was sind Nitrosylkomplexe
4. Carbonyl gegen Nitrosylkomplexe in tabellarischer Form
5. Zusammenfassung - Carbonyl gegen Nitrosylkomplexe
Was sind Carbonylkomplexe?
Carbonylkomplexe sind Koordinatenkomplexe, die aus Metallcenter und Carbonylliganden bestehen. Die Carbonylliganden, die wir hauptsächlich in diesen Komplexen finden können. Wir können Carbonylliganden häufig auch als Ausgangsmaterial für andere Koordinationsverbindungen verwenden. Dies erleichtert es einfach, eine Ligandensubstitution leicht durch das Reinigen des Reaktionsgefäßes zu machen.
Bei der Betrachtung der Bindung von -co -Liganden an ein Metallzentrum können wir feststellen, dass sie hauptsächlich durch die Bindungsbildung zwischen dem einzigen Elektronenpaar des CO -Moleküls und dem Metallzentrum auftritt. Hier fungiert der Co -Ligand als terminaler Ligand, weil es auf einer Seite nur eine chemische Bindung hat. Die Bindung des Co -Liganden erfolgt durch das Kohlenstoffatom des CO -Moleküls. Darüber hinaus kann das Teilen dieses einsamen Elektronenpaars zwischen einem, zwei oder sogar drei Metallzentren auftreten. Hier sollten diese Metallzentren mit Metallmetallbindungen miteinander verbunden sein. Wenn mehr als ein Metallzentrum an der Bildung von Carbonylkomplexen beteiligt ist, fungiert -co ligand als überbrückte Ligand. Wenn sich die beiden Metalle, die sich in der Metallmetallbindung befinden. In dieser Art von Situation fungiert Co-Ligand als Semi-Bridging-Ligand.
Darüber hinaus kann auch im Pi -Electron -Spendertyp in Carbonylkomplexen auftreten. Hier sind die PI -Elektronen des CO -Moleküls an der Elektronenspende an die Metallorbitale beteiligt. Diese Komplexe können diese Elektronen jedoch in der Konjugation mit dem Elektronenpaar der Kohlenstoffatome des Co -Liganden verwenden. Dies liegt daran.
Beispiele für Carbonylkomplexe
Einige Beispiele für Carbonylkomplexe sind:
- [CO (CO)6]3+
- [Fe (CO)6]2+
- [RH (CO)6]3+
- [Mn (CO)6]+
- [V (CO)6]-
Was sind Nitrosylkomplexe?
Nitrosylkomplexe sind Koordinatenkomplexe, die aus einem Metallzentrum und Stickoxidliganden bestehen, die bestehen. Die chemische Formel dieses Liganden ist -no, das an ein Übergangsmetallzentrum gebunden ist. Meistens tritt dieser Ligand als Nitrosylkation auf: Nein+. Dieses Kation ist isoelektronisch mit Co -Liganden. Daher haben die Bindung zwischen Metall und NO und die Bindung zwischen Metall und Co -Liganden die gleichen Eigenschaften.
Der No Ligand fungiert als Zwei-Elektronen-Spender, wo es das einzige Elektronenpaar mit dem Metallzentrum teilt. Darüber hinaus kann es Elektronen aus dem Metall durch den Hinterbindungsprozess akzeptieren. Im Zusammenhang mit der Elektronenzarstellung entsprechen zwei lineare Liganden jedoch chemisch drei linearen Co-Liganden.

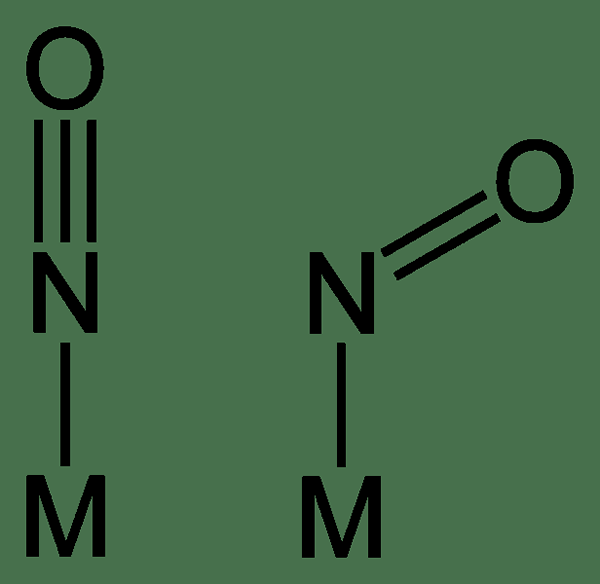
Abbildung 01: lineare und gebogene Nitrosylliganden
Darüber hinaus kann es lineare oder gebogene Nitrosylliganden geben. Linear kein Ligand hat drei kovalente Bindungen zwischen N- und O -Atomen, während kein Ligand zwei kovalente Bindungen zwischen N- und O -Atomen hat. Im Allgemeinen bildet der No -Ligand eine lineare Bindung zwischen dem Übergangsmetallzentrum und dem Liganden, während keine Liganden auftreten, wenn der Rückverbindungsprozess weniger wichtig ist.
Was ist der Unterschied zwischen Carbonyl- und Nitrosylkomplexen?
Carbonylkomplex und Nitrosylkomplex sind zwei Arten von Koordinationskomplexen, die ein Übergangsmetallzentrum und Liganden, die das Metallzentrum umgeben, enthalten. Der Hauptunterschied zwischen Carbonyl- und Nitrosylkomplexen besteht darin, dass Carbonylkomplexe -co -Liganden enthalten, während Nitrosylkomplexe -no -Liganden enthalten.
Die folgende Infografik listet die Unterschiede zwischen Carbonyl- und Nitrosylkomplexen in tabellarischer Form auf.
Zusammenfassung -Carbonyl gegen Nitrosylkomplexe
Carbonylkomplexe sind Koordinatenkomplexe, die aus Metallcenter und Carbonylliganden bestehen. Nitrosylkomplexe sind Koordinatenkomplexe, die aus einem Metallzentrum und Stickoxidliganden bestehen, die bestehen. Daher besteht der Hauptunterschied zwischen Carbonyl- und Nitrosylkomplexen darin, dass Carbonylkomplexe -co -Liganden enthalten, während Nitrosylkomplexe -no -Liganden enthalten.
Referenz:
1. “10.2: Prinzipien von Carbonylkomplexen“. Chemie -Libretexten.
Bild mit freundlicher Genehmigung:
1. "Metall-Nitrosyl-Coordination-Modes-2D" (Public Domain) über Commons Wikimedia


