Unterschied zwischen Ionenelektronenmethode und Oxidationszahlmethode
Der Schlüsselunterschied Zwischen der Ionenelektronenmethode und der Oxidationszahl -Methode besteht das, Bei der Ionenelektronenmethode ist die Reaktion abhängig von der Ladung der Ionen ausgeglichen, während bei der Oxidationszahl -Methode die Reaktion abhängig von der Änderung der Oxidationszahl von Oxidationsmitteln und Reduktionsmitteln ausgeglichen ist.
Sowohl die Ionenelektronenmethode als auch die Oxidationszahlmethode sind wichtig, um chemische Gleichungen auszugleichen. Für eine bestimmte chemische Reaktion wird eine ausgewogene chemische Gleichung angegeben und hilft uns zu bestimmen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Ionenelektronenmethode
3. Was ist die Oxidationszahlmethode
4. Seite für Seitenvergleich -Ionenelektronenmethode gegen Oxidationsnummer -Methode in tabellarischer Form
5. Zusammenfassung
Was ist Ionenelektronenmethode?
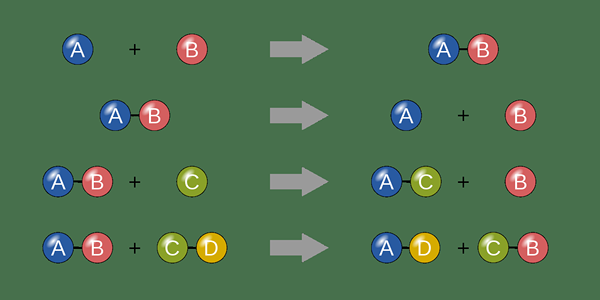
Die Ion-Elektronenmethode ist eine analytische Technik, mit der wir die stöchiometrische Beziehung zwischen Reaktanten und Produkten unter Verwendung ionischer Halbreaktionen bestimmen können. In Anbetracht der chemischen Gleichung für eine bestimmte chemische Reaktion können wir die beiden Halbreaktionen der chemischen Reaktion bestimmen und die Anzahl der Elektronen und Ionen in jeder halben Reaktion ausgleichen, um vollständig ausgeglichene Gleichungen zu erhalten.

Abbildung 01: Chemische Reaktionen
Betrachten wir ein Beispiel, um diese Methode zu verstehen.
Die Reaktion zwischen Permanganation und Eisenion ist wie folgt:
Mno4- + Fe2+ ⟶ mn2+ + Fe3+ + 4H2Ö
Die beiden Halbreaktionen sind die Umwandlung von Permanganation in Mangan (ii) Ion und Eisenion in Eisenion Ion. Die ionischen Formen dieser beiden Halbreaktionen sind wie folgt:
Mno4- ⟶ mn2+
Fe2+ ⟶ fe3+
Danach müssen wir die Anzahl der Sauerstoffatome in jeder halben Reaktion ausgleichen. In der halben Reaktion, bei der Eisen in Eisenion umgewandelt wird, gibt es keine Sauerstoffatome. Daher müssen wir den Sauerstoff in der anderen Halbreaktion ausgleichen.
Mno4- ⟶ mn2+ + 4o2-
Diese vier Sauerstoffatome stammen aus dem Wassermolekül (nicht aus molekularem Sauerstoff, da in dieser Reaktion keine Gasproduktion vorliegt). Dann ist die richtige Halbreaktion:
Mno4- ⟶ mn2+ + 4H2Ö
In der obigen Gleichung befinden sich keine Wasserstoffatome auf der linken Seite, aber es gibt acht Wasserstoffatome auf der rechten Seite, so dass wir der linken Seite acht Wasserstoffatome (in Form von Wasserstoffionen) hinzufügen müssen.
Mno4- + 8h+ ⟶ mn2+ + 4H2Ö
In der obigen Gleichung ist die ionische Ladung der linken Seite nicht gleich der rechten Seite. Daher können wir einem der beiden Seiten Elektronen hinzufügen, um die Ionische Ladung auszugleichen. Die Ladung auf der linken Seite beträgt +7 und auf der rechten Seite +2. Hier müssen wir fünf Elektronen zur linken Seite hinzufügen. Dann ist die halbe Reaktion,
Mno4- + 8h+ + 5e- ⟶ mn2+ + 4H2Ö
Beim Ausgleich der halben Reaktion der Eisen, die in Eisenwandung umgewandelt wird, wandelt sich die ionische Ladung von +2 auf +3 um; Hier müssen wir wie folgt ein Elektron zur rechten Seite hinzufügen, um die ionische Ladung auszugleichen.
Fe2+ ⟶ fe3+ + e-
Danach können wir zwei Gleichungen zusammen hinzufügen, indem wir die Anzahl der Elektronen ausbalancieren. Wir müssen die halbe Reaktion mit der Umwandlung von Eisen in Eisen mit 5 multiplizieren, um fünf Elektronen zu erhalten, und dann diese modifizierte Halbreaktionsgleichung zur Halbreaktion mit der Umwandlung von Permanganat in Mangan (II) Ion, die fünf Elektronen in jeder Seite stornieren ab. Die folgende Reaktion ist das Ergebnis dieser Zugabe.
Mno4- + 8h+ + 5FE2+ + 5e- ⟶ mn2+ + 4H2O + 5FE3+ + 5e-
Mno4- + 8h+ + 5FE2+ ⟶ mn2+ + 4H2O + 5FE3+
Was ist die Oxidationszahlmethode?
Die Oxidationszahlmethode ist eine analytische Technik, mit der wir die stöchiometrische Beziehung zwischen Reaktanten und Produkten bestimmen können. Bei einer Redoxreaktion gibt es zwei Halbreaktionen: Oxidationsreaktion und Reduktionsreaktion. Im gleichen Beispiel wie oben ist die Reaktion zwischen Permanganat und Eisenionen, Oxidationsreaktion die Umwandlung von Eisen in Eisenion, während die Reduktionsreaktion die Umwandlung von Permanganat in Mangan (II) Ion ist.
Oxidation: Fe2+ ⟶ fe3+
Reduktion: Mno4- ⟶ mn2+
Beim Ausgleich dieser Reaktionsart müssen wir zunächst die Änderung der Oxidationszustände chemischer Elemente bestimmen. In der Oxidationsreaktion wandelt sich +2 Eisenionen in +3 Eisenionionen um. Bei der Reduktionsreaktion konvertiert +7 Mangan in +2. Daher können wir die Oxidationszustände davon ausgleichen, indem wir die Halbreaktion mit dem Grad der Inkrement/Dekrementierung des Oxidationszustands in der anderen Halbreaktion multiplizieren. Im obigen Beispiel beträgt die Änderung des Oxidationszustands zur Oxidationsreaktion 1 und die Änderung des Oxidationszustands zur Reduktionsreaktion 5 beträgt 5. Dann müssen wir die Oxidationsreaktion mit 5 und die Reduktionsreaktion mit 1 multiplizieren.
5FE2+ ⟶ 5FE3+
Mno4- ⟶ mn2+
Danach können wir diese beiden Halbreaktionen hinzufügen, um die vollständige Reaktion zu erhalten, und dann die anderen Elemente (Sauerstoffatome) mit Wassermolekülen und Wasserstoffionen ausgleichen, um die ionische Ladung auf beiden Seiten auszugleichen.
Mno4- + 8h+ + 5FE2+ ⟶ mn2+ + 4H2O + 5FE3+
Was ist der Unterschied zwischen der Ionenelektronenmethode und der Oxidationszahlmethode?
Ionenelektronenmethode und Oxidationszahlmethode sind wichtig, um chemische Gleichungen auszugleichen. Der Schlüsselunterschied zwischen Ionenelektronenmethode und Oxidationszahlmethode besteht darin, dass die Reaktion bei der Ionenelektronenmethode abhängig von der Ladung der Ionen ausgeglichen ist, während die Reaktion bei der Oxidationszahl -Methode abhängig von der Änderung der Oxidationszahlen von Oxidationsmitteln und Reduktionen ausgeglichen ist.
Die folgende Infografik fasst den Unterschied zwischen der Ionenelektronenmethode und der Oxidationszahlmethode zusammen.

Zusammenfassung -Ionenelektronenmethode gegen Oxidationszahlmethode
Der Schlüsselunterschied zwischen Ionenelektronenmethode und Oxidationszahlmethode besteht darin, dass die Reaktion bei der Ionenelektronenmethode abhängig von der Ladung der Ionen ausgeglichen ist, während die Reaktion bei der Oxidationszahl -Methode abhängig von der Änderung der Oxidationszahlen von Oxidationsmitteln und Reduktionen ausgeglichen ist.
Referenz:
1. „Gleichungen ausbalancieren .” Org, 17 Apr. 2017, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Chemische Reaktionen" von Daniele Pugliesi - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia


