Unterschied zwischen ionischen und molekularen Verbindungen
Der Schlüsselunterschied Zwischen ionischen und molekularen Verbindungen befindet sich die Ionische Verbindungen haben elektrostatische Anziehungskräfte zwischen Kationen und Anionen, während die molekularen Verbindungen nur kovalente chemische Bindungen zwischen den Atomen aufweisen.
Chemische Elemente können sich miteinander verbinden, um chemische Verbindungen zu bilden. Die Elemente binden über chemische Bindungen mit ionischen oder kovalenten Eigenschaften. Wenn die Verbindungen ionische Bindungen haben, nennen wir sie als ionische Verbindungen, und wenn sie kovalente Bindungen haben, sind sie molekulare Verbindungen. Daher liegt der Schlüsselunterschied zwischen ionischen und molekularen Verbindungen in der chemischen Bindung zwischen Atomen.
INHALT
1. Überblick und wichtiger Unterschied
2. Whare sind ionische Verbindungen
3. Was sind molekulare Verbindungen
4. Seite an Seitenvergleich - ionische gegen molekulare Verbindungen in tabellarischer Form
5. Zusammenfassung
Was sind ionische Verbindungen?
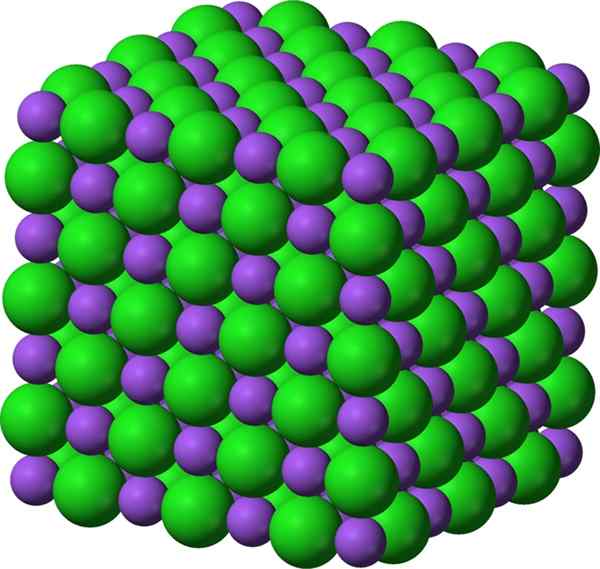
Ionenverbindungen sind die chemischen Verbindungen, die Kationen und Anionen haben, die über eine ionische Bindung aneinander binden. Daher gibt es elektrostatische Anziehungskräfte zwischen Kationen und Anionen. Die Verbindung hat jedoch eine insgesamt neutrale Ladung, da die Gesamtladung der Kationen durch die Gesamtladung der Anionen neutralisiert wird. Diese Ionen können entweder monoatomisch oder polyatomisch sein.
Normalerweise enthalten die ionischen Verbindungen, die Wasserstoffionen enthalten (H)+) Wie das Kation "Säuren" sind. Im Gegensatz dazu grundlegende Ionen wie Hydroxidion (OH-) ist in Basen vorhanden. Wenn es in der ionischen Verbindung keine Wasserstoffionen oder Hydroxidionen gibt, nennen wir es als „Salz“.

Abbildung 01: Ionische Verbindung von Natriumchlorid, ein Salz
Einige ionische Verbindungen wie Salze bilden sich aus Säure-Base-Neutralisationsreaktionen. Einige Verbindungen bilden sich durch Verdunstung des Lösungsmittels, Niederschlagsreaktionen, Festkörperreaktionen, Gefrierpunkte, Elektronentransferreaktionen zwischen Metallen und Nichtmetallen usw. Typischerweise haben diese Verbindungen hohe Schmelz- und Siedepunkte. Meistens sind sie hart und spröde. In ihrem Festzustand sind fast alle ionischen Verbindungen elektrische Isolatoren und können bei einem Lösungsmittel wie Wasser hoch leitend werden, weil sich die Kationen und Anionen frei bewegen können.
Was sind molekulare Verbindungen?
Molekulare Verbindungen sind chemische Verbindungen, die über kovalente chemische Bindungen Atome enthalten, die aneinander gebunden sind. Daher bilden sich diese Verbindungen, wenn Atome ihre ungepaarten Elektronen miteinander teilen. Die an dieser Elektronenfreigabe beteiligten Atome haben ähnliche Elektronegativitätswerte.
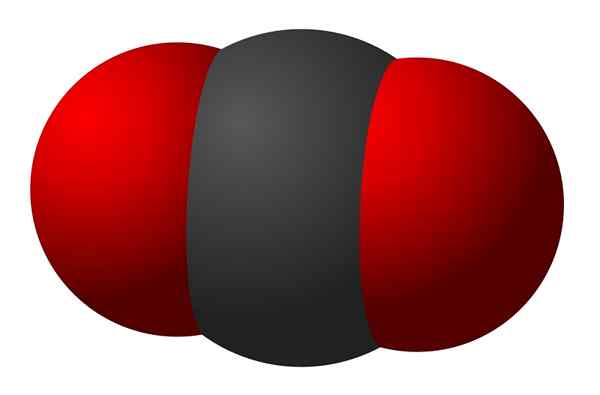
Abbildung 02: Ein Diagramm eines triatomischen Moleküls mit kovalenten Bindungen zwischen den drei Atomen
Typischerweise haben molekulare Verbindungen relativ geringe Schmelz- und Siedepunkte, da die Atome nicht stark aneinander befestigt sind. In ähnlicher Weise sind diese Verbindungen weich und relativ flexibel. Im Vergleich zu ionischen Verbindungen sind diese molekularen Verbindungen hoch entflammbar. Dies liegt daran, dass fast alle brennbaren Substanzen molekulare Verbindungen sind, die aus Kohlenstoff- und Wasserstoffatomen bestehen. Im Gegensatz zu ionischen Verbindungen können sie bei der Auflösung in einem Lösungsmittel keine Elektrizität leiten, da nach dem Auflösen keine Ionen verfügbar sind.
Was ist der Unterschied zwischen ionischen und molekularen Verbindungen?
Ionische Verbindungen sind die chemischen Verbindungen, die Kationen und Anionen haben, die über eine ionische Bindung aneinander binden, während molekulare Verbindungen chemische Verbindungen sind, die Atome enthalten. Daher liegt der Unterschied zwischen ionischen und molekularen Verbindungen auf der Art der chemischen Bindung. Das ist; Der Schlüsselunterschied zwischen ionischen und molekularen Verbindungen besteht darin, dass die ionischen Verbindungen elektrostatische Anziehungskräfte zwischen Kationen und Anionen haben, während die molekularen Verbindungen nur kovalente chemische Bindungen zwischen den Atomen aufweisen.
Als ein weiterer wichtiger Unterschied zwischen ionischen und molekularen Verbindungen sind die ionischen Verbindungen hart und spröde, während molekulare Verbindungen weich und relativ flexibel sind. Dies ist hauptsächlich daran zurückzuführen. Darüber hinaus sind die Schmelz- und Siedepunkte von ionischen Verbindungen im Vergleich zu molekularen Verbindungen sehr hoch.
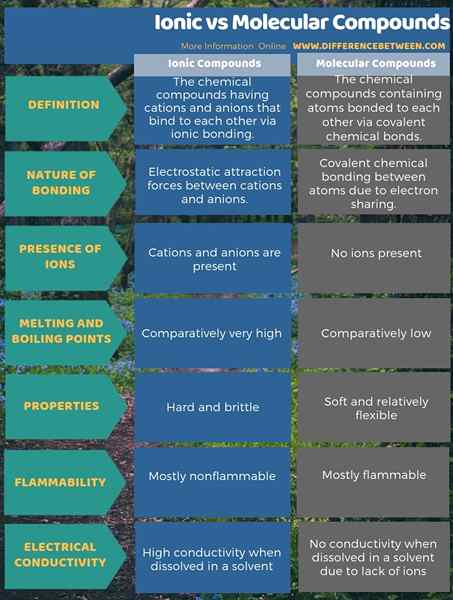
Zusammenfassung -ionische gegen molekulare Verbindungen
Ionenverbindungen haben ionische Bindungen, während molekulare Verbindungen kovalente Bindungen aufweisen. Der Schlüsselunterschied zwischen ionischen und molekularen Verbindungen besteht daher darin, dass die ionischen Verbindungen elektrostatische Anziehungskräfte zwischen Kationen und Anionen haben, während die molekularen Verbindungen nur kovalente chemische Bindungen zwischen den Atomen aufweisen.
Referenz:
1. Helmenstine, Anne Marie, ph.D. „Kovalente oder molekulare Verbindungseigenschaften.”Thoughtco, Jun. 7, 2018. Hier verfügbar
2. "Ionische Verbindung.”Wikipedia, Wikimedia Foundation, 20. Oktober. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Natriumchlorid-3D-Ionic” von Benjah-BMM27-eigene Arbeit, (gemeinfrei) über Commons Wikimedia
2.”Kohlendioxid-3D-VDW” von Jacek FH-eigene Arbeit (CC BY-SA 3.0) über Commons Wikimedia


