Unterschied zwischen Lithium und anderen Alkali -Metallen
Der Schlüsselunterschied Zwischen Lithium und anderen Alkali -Metallen ist das die Lithium ist das einzige Alkali -Metall, das mit Stickstoff reagieren kann, während die anderen Alkali -Metalle keine Reaktion mit Stickstoff durchführen können.
Alkali -Metalle sind die Elemente der Gruppe 1 der Periodenschaftstabelle von Elementen. Es schließt jedoch Wasserstoff aus, da es nichtmetallische Eigenschaften aufweist. Daher umfassen die chemischen Elemente, die wir als Alkali -Metalle nennen können. Obwohl Lithium Mitglied dieser Gruppe ist, hat es einige außergewöhnliche Eigenschaften als die anderen Alkali -Metalle wie die Fähigkeit, mit Stickstoffgas zu reagieren.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Lithium
3. Was sind andere Alkali -Metalle
4. Seite an Seitenvergleich - Lithium gegen andere Alkali -Metalle in tabellarischer Form
5. Zusammenfassung
Was ist Lithium?
Lithium ist ein Alkali -Metall mit der Atomzahl Nr. 3 und dem chemischen Symbol Li. Nach der Urknalltheorie der Erschaffung der Erde sind Lithium zusammen mit Wasserstoff und Helium die wichtigsten chemischen Elemente, die in den frühesten Stadien der Weltschöpfung produziert werden. Das Atomgewicht dieses Elements beträgt 6.941 und die Elektronenkonfiguration ist [er] 2s1. Darüber hinaus gehört es zum S -Block, da es sich in der Gruppe 1 der Periodenverkehrstabelle befindet und die Schmelz- und Siedepunkte dieses Elements 180 sind.50 ° C bzw. 1330 ° C. Es erscheint in silbrigweißer Farbe, und wenn wir dieses Metall verbrennen, gibt es eine purpurrote Flamme.

Abbildung 01: Lithiummetall
Dieses Metall ist sehr leicht und weich. Daher können wir es einfach mit einem Messer schneiden. Darüber hinaus kann es auf Wasser schwimmen, was zu einer explosiven chemischen Reaktion führt. Dieses Metall hat einige einzigartige Eigenschaften, die andere Alkali -Metalle nicht haben. Zum Beispiel ist es das einzige Alkali -Metall, das mit Stickstoffgas reagieren kann und bei dieser Reaktion Lithiumnitrid bildet. Es ist das kleinste Element unter anderen Mitgliedern dieser Gruppe. Darüber hinaus hat es die geringste Dichte zwischen festen Metallen.
Was sind andere Alkali -Metalle?
Alkali -Metalle sind die chemischen Elemente in Gruppe 1 der periodischen Elementtabelle mit Ausnahme von Wasserstoff. So sind die Mitglieder dieser Gruppen, die in diese Kategorie fallen. Der Grund, warum wir sie als Alkali -Metalle nennen, ist, dass sie Alkali -Verbindungen bilden.

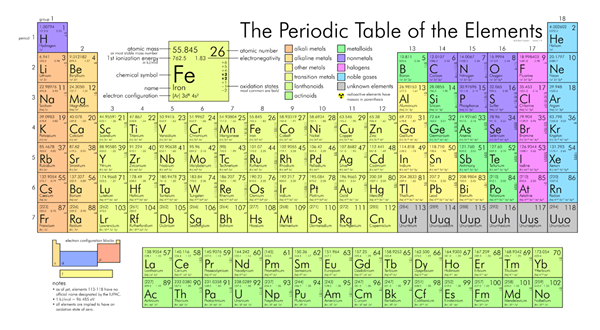
Abbildung 02: Alkali -Metalle in roten Farbe
Bei der Betrachtung der Elektronenkonfiguration haben sie ihr äußerstes Elektron in einem S -Orbital. Daher befinden sie sich im S -Block der Periodenzüchtertabelle. Die stabilste geladene Art, die sie bilden.
Was ist der Unterschied zwischen Lithium und anderen Alkali -Metallen?
Lithium ist ein Alkali -Metall mit der Atomzahlen Nummer 3 und des chemischen Symbols, während Alkali -Metalle die chemischen Elemente in Gruppe 1 der Periodenlinge der Elemente mit Ausnahme von Wasserstoff sind. Der Hauptunterschied zwischen Lithium und anderen Alkali -Metallen besteht darin, dass das Lithium das einzige Alkali -Metall ist, das mit Stickstoff reagieren kann. Darüber hinaus kann Lithium kein Anion bilden, während andere Alkali -Metalle Anionen bilden können.
Der folgende Infografik tabelt den Unterschied zwischen Lithium und anderen Alkali -Metallen als Nebeneinander -Vergleich auf.
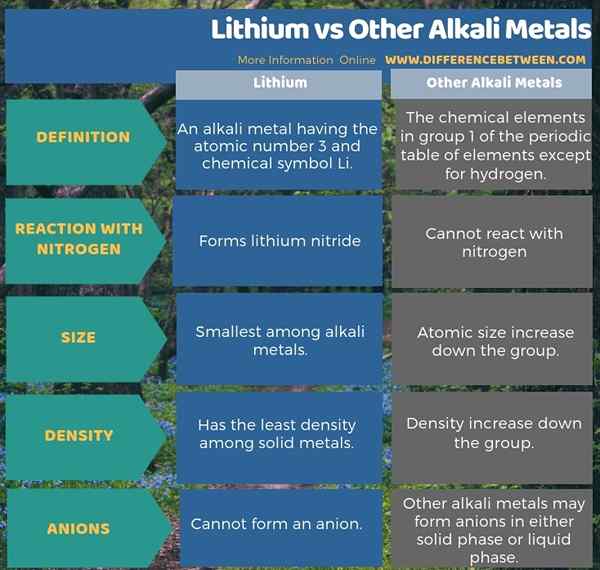
Zusammenfassung -Lithium gegen andere Alkali -Metalle
Lithium ist Mitglied der Gruppe der Alkali -Metalle. Der Hauptunterschied zwischen Lithium und anderen Alkali -Metallen besteht darin, dass das Lithium das einzige Alkali -Metall ist, das mit Stickstoff reagieren kann.
Referenz:
1. "Lithium.Wikipedia, Wikimedia Foundation, 30. September. 2018. Hier verfügbar
2. "Alkalimetall.Wikipedia, Wikimedia Foundation, 11. September. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1."Lithium paraffin" von Tomihahndorf (Public Domain) über Commons Wikimedia
2.”Periodenzüchter von Elementen“ von 2012RC - eigene Arbeit (Public Domain) über Commons Wikimedia


