Unterschied zwischen Methylacetat und Ethylacetat
Der Schlüsselunterschied zwischen Methylacetat und Ethylacetat ist das Methylacetat hat eine Methylgruppe, die an eine Acetatgruppe gebunden ist, während Ethylacetat eine Ethylgruppe an einer Acetatgruppe gebunden ist.
Acetat ist ein aus der Essigsäure abgeleiteter Anionen (die Entfernung des Wasserstoffatoms in der Carboxylsäuregruppe bildet das Acetatanion). Sowohl Methylacetat als auch Ethylacetat sind organische Verbindungen mit eng verwandten chemischen und physikalischen Eigenschaften.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Methylacetat
3. Was ist Ethylacetat
4. Ähnlichkeiten zwischen Methylacetat und Ethylacetat
5. Seite für Seitenvergleich -Methylacetat gegen Ethylacetat in tabellarischer Form
6. Zusammenfassung
Was ist Methylacetat?
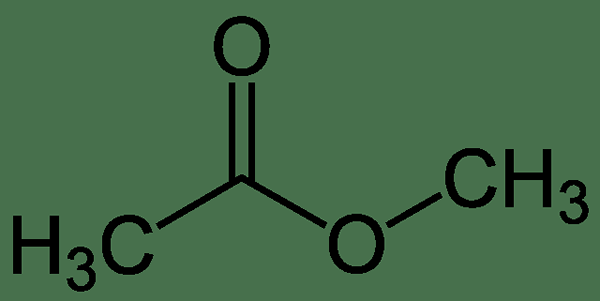
Methylacetat ist eine organische Verbindung mit der chemischen Formel CH3Cooch3. Hier das Acetat (-Cooch3) Gruppe ist an eine Methylgruppe (-ch) gebunden3). Die Molmasse der Verbindung beträgt 74 g/mol. Es wird als Carboxylatester eingestuft.

Abbildung 1: Methylacetat
Bei Raumtemperatur ist Methylacetat eine farblose Flüssigkeit mit einem duftenden Geruch. Es hat auch einen fruchtigen Geschmack. Der Schmelzpunkt dieser Verbindung beträgt -98 ° C, während der Siedepunkt 56 beträgt.9 ° C. Diese Verbindung ist mäßig toxisch. Es ist auch eine brennbare Flüssigkeit und hat einige Verwendungszwecke als Lösungsmittel. Darüber hinaus ist es ein schwach polares und lipophiles Lösungsmittel. Bei Raumtemperatur ist Methylacetat schlecht wasserlöslich. Bei höheren Temperaturen hat die Verbindung jedoch eine hohe Wasserlöslichkeit. Darüber hinaus sind Methylacetatdämpfe schwerer als normale Luft.
Was ist Ethylacetat?
Ethylacetat ist eine organische Verbindung mit der chemischen Formel CH3CH2Cooch3. Die Molmasse dieser Verbindung beträgt 88 g/mol. Es wird als Carboxylatester eingestuft, da Ethylacetat durch die Wechselwirkung zwischen Carboxylatgruppe und einer Ethylgruppe gebildet wird, wobei eine Esterbindung bildet. Darüber hinaus ist Ethylacetat der Ester von Ethanol und Essigsäure.
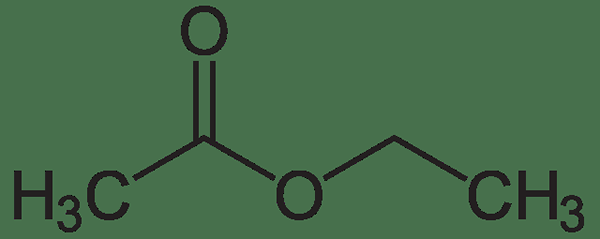
Abbildung 2: Ethylacetat
Bei Raumtemperatur ist Ethylacetat eine farblose Flüssigkeit mit fruchtigem Geruch. Diese Flüssigkeit wird auch häufig als Lösungsmittel verwendet. Ethylacetatdampf ist schwerer als normale Luft. Es gibt eine breite Palette von Anwendungen für diese Flüssigkeit aufgrund seiner günstigen Kosten, seiner geringen Toxizität und des angenehmen Geruchs.
Der Schmelzpunkt von Ethylacetat beträgt -83.6 ° C, während der Siedepunkt 77 ° C beträgt. Es ist eine brennbare Flüssigkeit und ein Reizmittel. Darüber hinaus führt die Hydrolyse von Ethylacetat zu Essigsäure und Ethanol. Diese Hydrolyse ist ein zweistufiger Prozess, der in Gegenwart einer starken Basis wie Natriumhydroxid (NaOH) auftritt. Der erste Schritt beinhaltet die Bildung von Ethanol und Natriumacetat, während der zweite Schritt die Umwandlung von Natriumacetat in Essigsäure umfasst.
Was sind die Ähnlichkeiten zwischen Methylacetat und Ethylacetat?
- Methylacetat und Ethylacetat sind farblose Flüssigkeiten bei Raumtemperatur mit fruchtigem, angenehmem Geruch.
- Sowohl Methylacetat als auch Ethylacetat sind brennbar.
- Beide Verbindungen sind Carboxylatester.
- Methylacetat und Ethylacetat werden als Lösungsmittel verwendet.
Was ist der Unterschied zwischen Methylacetat und Ethylacetat?
Methylacetat gegen Ethylacetat | |
| Methylacetat ist eine organische Verbindung mit der chemischen Formel CH3Cooch3. | Ethylacetat ist eine organische Verbindung mit der chemischen Formel CH3CH2Cooch3. |
| Molmasse | |
| Die Molmasse von Methylacetat beträgt 74 g/mol. | Die Molmasse von Ethylacetat beträgt 88 g/mol. |
| Schmelz- und Siedepunkte | |
| Der Schmelzpunkt von Methylacetat beträgt -98 ° C, während der Siedepunkt 56 beträgt.9 ° C. | Der Schmelzpunkt von Ethylacetat beträgt -83.6 ° C, während der Siedepunkt 77 ° C beträgt. |
| Toxizität | |
| Methylacetat ist mäßig toxisch. | Ethylacetat ist weniger toxisch als Methylacetat. |
| Als Lösungsmittel verwenden | |
| Methylacetat wird nur gelegentlich als Lösungsmittel verwendet. | Ethylacetat wird häufiger als Lösungsmittel verwendet. |
Zusammenfassung -Methylacetat gegen Ethylacetat
Sowohl Methylacetat als auch Ethylacetat sind organische Verbindungen mit eng verwandten chemischen und physikalischen Eigenschaften. Der Schlüsselunterschied zwischen Methylacetat und Ethylacetat besteht darin, dass Methylacetat eine Methylgruppe auf eine Acetatgruppe aufweist, während Ethylacetat eine Ethylgruppe auf eine Acetatgruppe aufweist.
Referenz:
1. „Methylacetat.Nationales Zentrum für Biotechnologieinformationen. Pubchem Compound -Datenbank, u.S. National Library of Medicine, hier verfügbar.
2. „Methylacetat.”Wikipedia, Wikimedia Foundation, 14. April. 2018, hier erhältlich.
3. "Ethylacetat.”Wikipedia, Wikimedia Foundation, 10 April. 2018, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Methylacetat-Strukturformel v1" von Jü-eigener Arbeit (CC BY-SA 4.0) über Commons Wikimedia
2. "Essigsäureethylester" von Neurotiker (Talk) - eigene Arbeit (Public Domain) über Commons Wikimedia


