Unterschied zwischen MNO2 und CUO

Der Schlüsselunterschied Zwischen Mno2 und Cuo ist das MnO2 ist das Oxid von Mangan, während Cuo das Kupferoxid ist.
MNO2 und CuO sind anorganische Verbindungen, die ein ähnliches Aussehen haben und als schwärzbraune Feststoffe bei Raumtemperatur vorhanden sind. Daher ist es sehr schwierig, diese beiden festen Verbindungen zu unterscheiden, indem wir sie ansehen. Daher benötigen wir unterschiedliche experimentelle Verfahren, um sie separat zu identifizieren. Als grundlegender Unterschied haben sie unterschiedliche chemische Zusammensetzungen; MNO2 hat Mangan in seiner Oxidform, während die Cuo -Verbindung Kupfer in ihrer Oxidform hat, die das Kupfer im +2 -Oxidationszustand hat.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Mno2
3. Was ist cuo
4. Nebenseitiger Vergleich - Mno2 gegen Cuo in tabellarischer Form
5. Zusammenfassung
Was ist Mno2?
MNO2 ist Mangan (IV) Oxid, das Mangan im Oxidationszustand von +4 hat. Es erscheint bei Raumtemperatur als schwärzbraunen Feststoff. Natürlich kommt es in der Mineralform Pyrolusit auf. Der bevorzugte IUPAC -Name für diese Verbindung ist Mangan (IV) Oxid. Die Molmasse von MnO2 beträgt 87 g/mol. Es ist ein wasserunlösliches Feststoff. Es gibt mehrere Anwendungen von MNO2. Es ist hauptsächlich als Komponente in trockenen Zellbatterien nützlich. Außerdem ist es in der organischen Synthese als Oxidationsmittel wichtig.
Es sind einige bekannte Polymorphen und hydratisierte Formen von MNO2. Darüber hinaus kristallisiert diese Verbindung in Form einer Rutilkristallstruktur. Es hat ein oktaedrisches Metallzentrum und drei koordinierte Oxide.

Es gibt zwei mögliche Produktionsmethoden des Mangans -Dioxids (MNO2); Sie sind die chemische Methode und die elektrolytische Methode. Die chemische Methode beginnt mit natürlichen Mangandioxid, das Verunreinigungen aufweist. Wir müssen diesen natürlichen MnO2 mit Dinitrogen -Tetroxid mit Wasser in Mangan (ii) Nitrat umwandeln. Nach dem Erhitzen verdunstet das Nitratsalz und freisetzt n n2Ö4, und wir können das verbleibende Mangandioxid beobachten, das in der reinen Form ist. Die elektrolytische Methode ist auch eine nützliche Methode bei der Herstellung von MNO2. Hier sind reine Mangan -Dioxidablagerungen auf der Anode Ablagerungen.
Was ist cuo?
Cuo ist Kupfer (II) Oxid. Es hat Kupfer im +2 Oxidationszustand. Es erscheint bei Raumtemperatur als schwärzbraunen Feststoff. Es ist eines der beiden stabilsten Kupferoxide. In der Natur tritt Kupferoxid in einer Mineralform auf, die als Tenorit bezeichnet wird. Der IUPAC -Name dieser Verbindung ist Kupfer (II) Oxid. Die Molmasse ist 79.5 g/mol. Es ist wasserunlöslich. Darüber hinaus hat es eine monokline Kristallstruktur. Hier assoziiert ein Kupferatom mit vier Sauerstoffatomen in einer quadratplanaren Geometrie.

Pyrometallurgie ist die Methode, die wir üblicherweise für die Produktion von Cuo verwenden. Hier können wir Kupferoxid aus seinem Erz extrahieren. In diesem Prozess müssen wir das Erz mit einer Mischung aus wässrigem Ammoniumcarbonat, Ammoniak und Sauerstoff behandeln. Diese Behandlung ergibt zunächst Kupfer (i) und Kupfer (II) Amminkomplexe. Dann können wir diese Komplexe zersetzen, um reines Cuo zu bekommen. Darüber hinaus können wir diese Verbindung auch in Gegenwart von Sauerstoff über das Erhitzen von Kupfermetall produzieren.
Was sind die Ähnlichkeiten zwischen MnO2 und Cuo?
- Sowohl Mno2 als auch Cuo haben das gleiche Erscheinungsbild wie schwarzbrauner Farbe, und sie existieren in der festen Phase bei Raumtemperatur.
- Diese Verbindungen sind in Wasser unlöslich.
Was ist der Unterschied zwischen Mno2 und Cuo?
Der Hauptunterschied zwischen Mno2 und Cuo besteht darin, dass MnO2 das Oxid von Mangan ist, während Cuo das Kupferoxid ist. Darüber hinaus befindet sich das Metallatom in MnO2 im +4 -Oxidationszustand, während in Cuo das Metallatom im +2 -Oxidationszustand liegt.
Darüber hinaus besteht ein weiterer Unterschied zwischen Mno2 und Cuo darin, dass MnO2 eine rutile Kristallstruktur aufweist, während Cuo eine monokline Struktur hat.
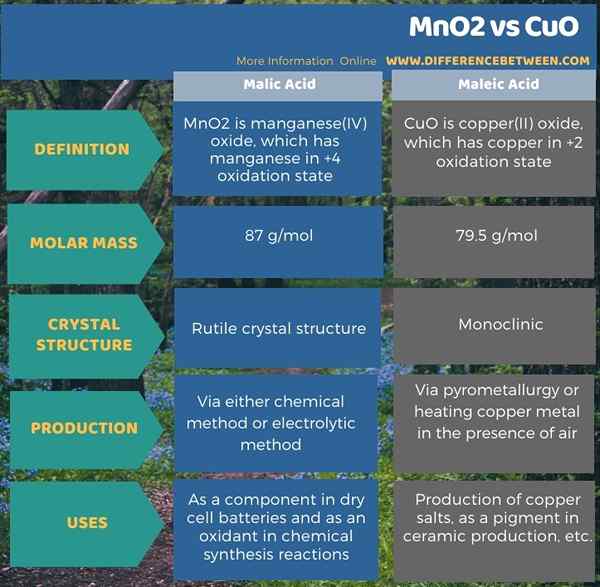
Zusammenfassung -Mno2 gegen Cuo
Sowohl Mno2 als auch Cuo haben das gleiche Erscheinungsbild wie schwarzbrauner Farbe, und sie existieren in der festen Phase bei Raumtemperatur. Der Hauptunterschied zwischen Mno2 und Cuo besteht darin, dass MnO2 das Oxid von Mangan ist, während Cuo das Kupferoxid ist.
Referenz:
1. Helmenstine, Anne Marie. „Mangan Fakten.”Thoughtco, Jul. 3, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Mangan (iv) Oxid" von Walkerma Angenommen - keine maschinenlesbare Quelle zur Verfügung gestellt. Eigene Arbeit angenommen (basierend auf Urheberrechtsansprüchen) (öffentlich zugänglich) über Commons Wikimedia
2. "Copperiioxid" von User Walkerma auf En EN.Wikipedia, Public Domain) über Commons Wikimedia


