Unterschied zwischen Olefinen und Paraffinen
Der Schlüsselunterschied Zwischen Olefins und Paraffins ist das Olefine enthalten im Wesentlichen eine oder mehrere Doppelbindungen zwischen Kohlenstoffatomen, während Paraffine keine doppelte oder dreifache Bindung zwischen Kohlenstoffatomen enthalten.
Olefin und Paraffin sind häufige Begriffe für zwei verschiedene Gruppen von Kohlenwasserstoffverbindungen. Olefine sind Alkene, und Paraffine sind Alkane. Diese beiden Begriffe Olefin und Paraffin werden hauptsächlich in industriellen Anwendungen verwendet.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind Olefine?
3. Was sind Paraffine
4. Seite an Seitenvergleich - Olefins gegen Paraffine in tabellarischer Form
5. Zusammenfassung
Was sind Olefine??
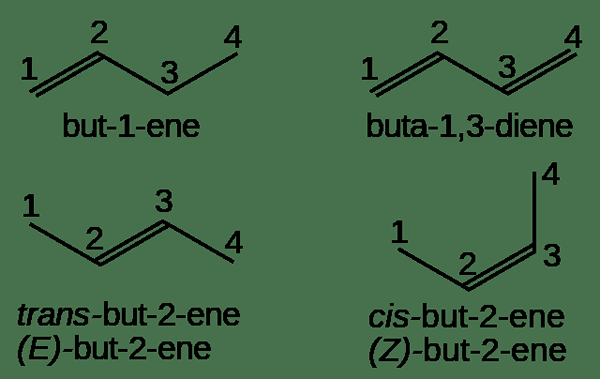
Olefine sind Alkene. Sie enthalten eine oder mehrere Doppelbindungen zwischen Kohlenstoffatomen. Ein Olefin ist eine Gruppe von Kohlenwasserstoffen, die nur aus Kohlenstoff- und Wasserstoffatomen bestehen. Olefin ist ein anderer Name für Alkene, da Olefine Kohlenwasserstoffe sind, die aus Kohlenstoffatomen mit Doppelbindungen bestehen. Daher bestehen Olefine aus SP3 Hybridisierte Kohlenstoffatome sowie SP2 Hybridisierte Kohlenstoffatome. Darüber hinaus sind sie ungesättigte Kohlenwasserstoffverbindungen.
Olefine haben C-H-Einzelbindungen, C-C-Einzelbindungen und C = C-Doppelbindungen. Es kann verschiedene Kombinationen von Kohlenstoff- und Wasserstoffatomen geben. Aber all diese Kombinationen werden durch die allgemeine Formel von Olefinen dargestellt, nämlich cNH2n wobei n eine ganze Zahl ist.

Abbildung 01: Olefine
Olefine können auf verschiedene Arten kategorisiert werden. Zyklische Strukturen werden als zyklische Olefine bezeichnet. Aliphatische Strukturen werden als acyclische Olefine bezeichnet. Nach der Anzahl der Doppelbindungen, die in der chemischen Struktur vorhanden sind, können Olefine als Monoolefine, Diolefine, Triolefine usw. bezeichnet werden.
Olefine finden Sie in allen drei Phasen der Materie in Abhängigkeit von ihren chemischen Strukturen. Einfache Olefine existieren als Gase, während komplexe Olefine als Flüssigkeiten oder Feststoffe existieren. Aufgrund ihrer hohen chemischen Reaktivität treten Olefine in sehr begrenzten Mengen an Rohöl und Erdgasen auf. Olefine können in Raffinerien während der Rohölverarbeitung hergestellt werden. Hier werden Olefine durch Cracking -Prozesse erzeugt. Zum Beispiel ist thermisches Risse eine Hauptreaktion, mit der Olefine aus Erdölöl erhalten werden können.
Was sind Paraffine?
Paraffine sind Alkane, die gesättigte Kohlenwasserstoffe mit der chemischen Formel C sindNH2n+2 (wobei n eine ganze Zahl ist). Diese werden Kohlenwasserstoffe genannt, weil sie C- und H -Atome enthalten. Alle diese Atome sind über einzelne kovalente Bindungen miteinander verbunden. Da es keine Doppel- oder Dreifachbindungen gibt, sind Paraffine gesättigte Kohlenwasserstoffe.
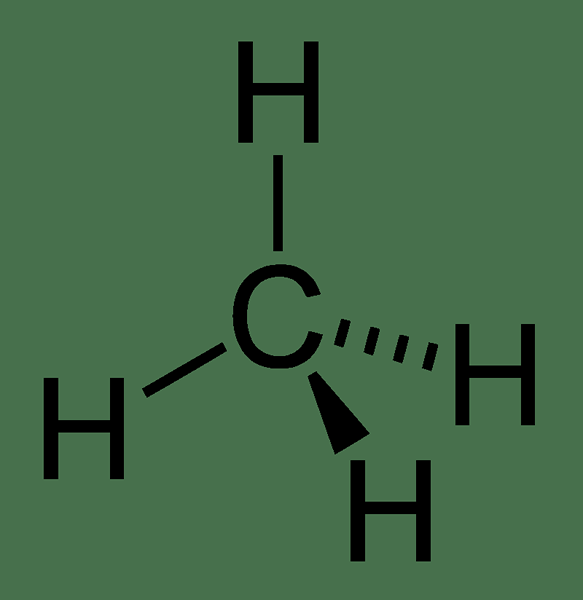
Abbildung 02: Methan, ein einfaches Paraffin
Darüber hinaus sind diese Verbindungen eine breite Gruppe von organischen Molekülen. Wir können sie gemäß der Anzahl der Kohlenstoffatome und der Seitengruppen nennen, aus denen sie bestehen. Das kleinste Alkan ist Methan. In Methan bindet ein zentrales Kohlenstoffatom mit 4 Wasserstoffatomen. Die IUPAC -Nomenklatur von Paraffins basiert auf griechischen Präfixen.
Alle Paraffine sind farblos und geruchlos. Die Schmelzpunkte und Siedepunkte steigen mit zunehmender Anzahl von Kohlenstoffatomen. Unter Standardtemperatur- und Druckbedingungen sind einige von ihnen Flüssigkeiten, während einige gasförmige Verbindungen sind. Und dieser Unterschied ist auf ihre unterschiedlichen Siedepunkte zurückzuführen. Darüber hinaus zeigen Alkane Isomerismus. Ein Paraffinmolekül kann strukturelle Isomerismus oder Stereoisomerismus entsprechend seiner Struktur und räumlichen Anordnung des Moleküls haben.
Was ist der Unterschied zwischen Olefins und Paraffinen?
Olefin und Paraffin sind häufige Begriffe für zwei verschiedene Gruppen von Kohlenwasserstoffverbindungen. Olefine sind Alkene, während Paraffine Alkane sind. Daher besteht der Hauptunterschied zwischen Olefinen und Paraffinen darin, dass Olefine im Wesentlichen eine oder mehrere Doppelbindungen zwischen Kohlenstoffatomen enthalten, während Paraffine keine doppelte oder dreifache Bindung zwischen Kohlenstoffatomen enthalten. Darüber hinaus ist die allgemeine Formel für Olefine CNH2N, während die Formel für Paraffine CNH2N+2 ist. Darüber hinaus können Olefine aufgrund des Vorhandenseins von PI -Bindungen einer Polymerisation durchlaufen, aber Paraffine können aufgrund des Fehlens von PI -Bindungen keine Polymerisation durchlaufen.
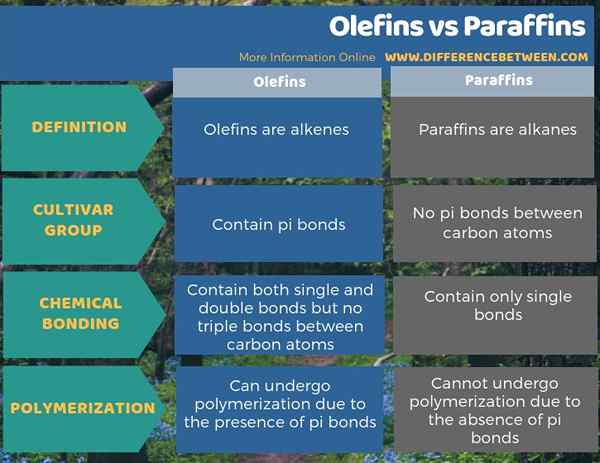
Zusammenfassung -Olefins gegen Paraffine
Der Begriff Olefin und Paraffin sind häufige Begriffe für zwei verschiedene Gruppen von Kohlenwasserstoffverbindungen. Olefine sind Alkene, und Paraffine sind Alkane. Daher besteht der Hauptunterschied zwischen Olefinen und Paraffinen darin, dass Olefine im Wesentlichen eine oder mehrere Doppelbindungen zwischen Kohlenstoffatomen enthalten, während Paraffine keine doppelte oder dreifache Bindung zwischen Kohlenstoffatomen enthalten.
Referenz:
1. „Paraffinkohlenwasserstoff.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., Hier verfügbar.
Bild mit freundlicher Genehmigung:
1. "IUPAC-ALKENE" von fvasconcellos 20:06, 8. Januar 2008 (UTC). Originalbild von DRBOB (Talk · Beiträge). - Vektorversion von Bild: IUPAC-ALKENE.PNG von DRBOB (talk · Beiträge) (CC BY-SA 3.0) über Commons Wikimedia
2. "Methane-2D-Stereo" von SVG-Version von Patricia.FIDI - eigene Arbeit (Public Domain) über Commons Wikimedia


