Unterschied zwischen Singulett und Triplettcarbän
Der Schlüsselunterschied Zwischen Singulett und Triplet Carbe ist das die Singulettcarbänes sind Spinpaare, während die Triplettcarbenen zwei ungepaarte Elektronen haben.
Ein Carben ist eine funktionelle Gruppe in der organischen Chemie. Es hat zwei Valenzschalenelektronen, die nicht an einer Bindung teilnehmen. Die allgemeine Formel für diese Gruppe ist r- (c:) -R 'oder r = c: in dem das „R“ entweder ein Wasserstoffatom oder ein Alkylsubstituenten ist. In Abhängigkeit von der elektronischen Struktur können wir Carbenen in zwei Gruppen als Singlets oder Drillinge eintreffen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Singulet Carbene
3. Was ist Triplet Carbe
4. Nebenseitiger Vergleich - Singulett gegen Triplettcarbän in tabellarischer Form
5. Zusammenfassung
Was ist Singulet Carbene?
Singulett Carben ist eine Form der Carben -Gruppe, die keine ungepaarten Elektronen hat. Daher nennen wir es als "Spinpaar-Carbän". Der Gesamtdreh dieser Gruppen ist Null. Diese Art der Carbän -Gruppe hat eine SP2 -Hybridstruktur. Diese sind diamagnetisch, weil es keine ungepaarten Elektronen gibt. Darüber hinaus verfügt die Singulet Carben Group über einen Bindungswinkel von 102 °. Diese Gruppen treten häufiger in wässrigen Medien auf, da diese in einem gasförmigen Zustand nicht stabil sind.

Abbildung 01: Das einfachste Carbän ist Methylen
Bei der Betrachtung der Reaktivität der Singulett -Carbengruppe beteiligen sie sich im Allgemeinen an cheletropen Reaktionen, indem sie entweder als Elektrophil oder als Nucleophile fungieren. Daher sind die Reaktionen von ihnen stereospezifisch.
Was ist Triplet Carbe?
Triplet Carben ist eine Form der Carben -Gruppe mit zwei ungepaarten Elektronen. Die Geometrie dieser Gruppe kann entweder linear oder gebogen sein. Wenn es sich um eine lineare Geometrie handelt, hat es die SP -Hybridstruktur. Aber wenn es eine gebogene Geometrie ist, hat es eine SP2 -Hybridstruktur. In den meisten Fällen weist das Triplettcarbän jedoch eine nichtlineare Geometrie auf, mit Ausnahme derjenigen mit Stickstoff, Sauerstoff oder Schwefelatomen. Darüber hinaus beträgt der Bindungswinkel für diese Gruppen 125-140 °.

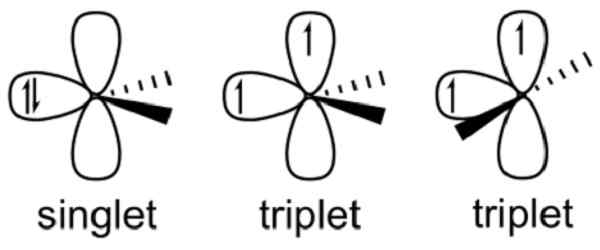
Abbildung 02: Unterschied zwischen Singulett- und Triplett -Carben -Geometrien
Aufgrund des Vorhandenseins von Triplettkarben sind sie paramagnetisch. Daher können wir sie über Elektronenspin -Resonanzspektroskopie beobachten. Der gesamte Dreh dieser Carbänes ist eins. Im Allgemeinen sind diese Gruppen in ihrem gasförmigen Zustand stabil. Bei der Betrachtung der Reaktivität von Triplettkarben fungieren sie als Diradicals und können an schrittweisen radikalen Reaktionen teilnehmen. Im Gegensatz zu Singulett -Carben müssen diese Triplett -Carbenen jedoch ein Zwischenprodukt mit zwei ungepaarten Elektronen durchlaufen. Die Reaktionen, die sie unterziehen, sind stereoselektiv.
Was ist der Unterschied zwischen Singulett und Triplettcarbän?
Carbene sind organische funktionelle Gruppen mit der chemischen Formel R- (C:) -R 'oder r = c: Je nach elektronischer Struktur gibt es zwei Formen von Carbenen als Singulett -Carbän und Triplettcarbän. Daher besteht der wesentliche Unterschied zwischen Singulett und Triplett-Carbän darin, dass Singulett-Carbene Spinpaare sind, während Triplettcarbene zwei ungepaarte Elektronen haben. Es gibt viele andere Unterschiede zwischen Singulett -Carbän und Triplettcarbän wie den Unterschieden in ihrer Geometrie, Hybridstrukturen, Gesamtspin, Bindungswinkel, magnetischen Eigenschaften usw.
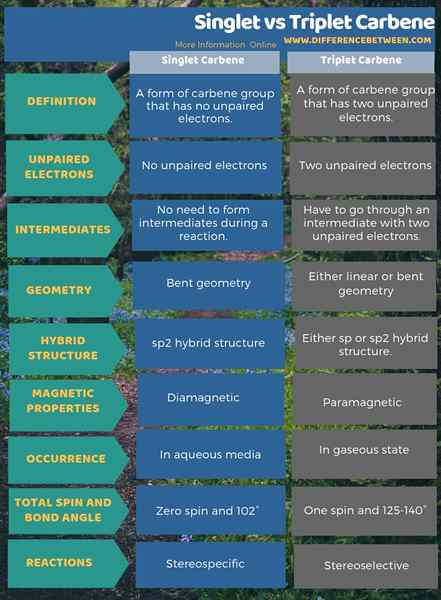
Das folgende inforgraphische enthält weitere Informationen über den Unterschied zwischen Singulett und Triplettcarbän in tabellarischer Form.
Zusammenfassung -Singlet vs Triplett Carbe
Carben ist in zwei Haupttypen als Singulett Carbe und Triplett Carbe nach ihrer elektronischen Struktur. Der wichtigste Unterschied zwischen Singulett und Triplettcarbän besteht darin, dass die Singulet-Carbene Spinpaare sind, während die Triplettcarbenen zwei ungepaarte Elektronen haben.
Referenz:
1. „Carbenes.”Chemistry Libretexten, Libretexte, 21. Juli 2016. Hier verfügbar
2. „Carbe.Wikipedia, Wikimedia Foundation, 24. September. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Carbe” von HBF878 - eigene Arbeit (CC0) über Commons Wikimedia
2."Carbenes" von HBF878 - eigene Arbeit, (CC0) über Commons Wikimedia