Unterschied zwischen THF und Dioxan

Der Schlüsselunterschied Zwischen THF und Dioxan ist das THF -Moleküle enthalten ein Sauerstoffatom als Mitglied der Ringstruktur, während das Dioxanmolekül zwei Sauerstoffatome als Mitglieder der Ringstruktur enthält.
Sowohl THF als auch Dioxan sind organische Lösungsmittel, die für die Analyse von Proben wichtig sind. Diese organischen Strukturen sind zyklische Strukturen, die wir als heterocyclische Verbindungen klassifizieren können, da diese Ringstrukturen zwei Arten von Atomen enthalten, die den Ring bilden: Kohlenstoffatome und Sauerstoffatom (en).
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist thf
3. Was ist Dioxan
4. Seite an Seite Vergleich - THF gegen Dioxan in tabellarischer Form
5. Zusammenfassung
Was ist thf?
THF ist ein organisches Lösungsmittel mit der chemischen Formel (CH2) 4O. Es handelt sich um eine heterocyclische Verbindung, und wir können sie als Ether kategoralisieren-. Wir können THF als farblose organische Flüssigkeit beobachten, die mit Wasser mischbar ist. Dieses Lösungsmittel hat einen ätherähnlichen Geruch. Es hat auch eine niedrige Viskosität. Dieses Lösungsmittel wird hauptsächlich als Vorläufer für Polymersyntheseprozesse verwendet. THF ist ein polares Molekül, das beim Mischen mit Wasser hilfreich ist. Zusätzlich zu diesen macht diese Polarität zu einem vielseitigen Lösungsmittel.

Abbildung 01: THF Lösungsmittel
Bei der Betrachtung der Anwendungen des THF -Lösungsmittels ist dies bei Polymerisationsprozessen wichtig. In Gegenwart starker Säuren konvertiert THF in ein lineares Polymermaterial, Poly (Tetramethylenether) Glykol oder PTMEG. Dieses Polymermaterial ist nützlich bei der Herstellung von elastomeren Polyurethanfasern wie Spandex.
Darüber hinaus ist THF als Lösungsmittel für PVC und Lack wichtig. Dies liegt daran, dass THF ein aprotisches Lösungsmittel mit einer Dielektrizitätskonstante von 7 ist.6. Wir können THF als mäßig polares Lösungsmittel einstufen, das einen weiten Bereich von nichtpolaren und polaren chemischen Verbindungen auflösen kann.
Darüber hinaus ist THF als Komponente in der mobilen Phase für die Flüssigkeitschromatographie umgekehrter Phase nützlich. THF wird in dieser Technik verwendet.
Was ist Dioxan?
Dioxan ist eine heterocyclische organische Verbindung mit der chemischen Formel C4H8O2. Wir können es als Äther klassifizieren. Es existiert als farblose Flüssigkeit mit einem milden ätherähnlichen Geruch. Es gibt drei Isomere von Dioxan als 1,2-Dioxan, 1,3-Dioxan und 1,4-Dioxan. Unter diesen drei Verbindungen ist 1,4-dioxan die gemeinsame Verbindung, bei der andere Verbindungen selten auftreten.
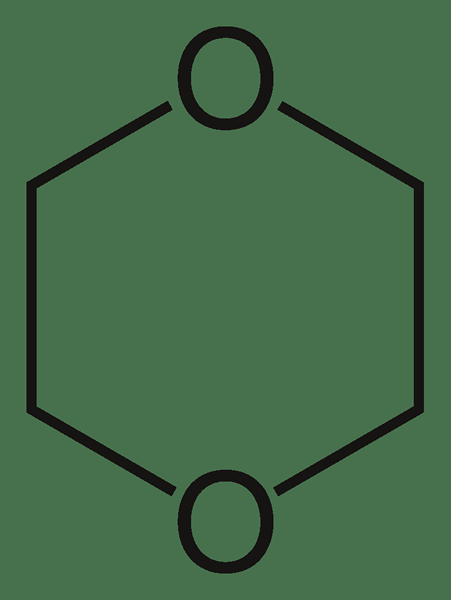
Abbildung 02: Struktur des Dioxanmoleküls
Bei der Betrachtung der Synthese kann Dioxan über die säurebatalysierte Dehydration von Diethylenglykol produziert werden. Wir können Diethylenglykol aus der Hydrolyse von Ethylenoxid erhalten. Diese Flüssigkeit ist mit Wasser mischbar, weil sie polar ist.
Dioxan ist im Trichlorethantransport als Stabilisator wichtig. Darüber hinaus ist es als aprotisches Lösungsmittel für Tinten, Klebstoffe und Celluloseester wichtig. Wir können dieses Lösungsmittel in einigen Prozessen aufgrund der geringen Toxizität und des hohen Siedepunkts des dioxanischen Lösungsmittels als Ersatz von THF verwenden.
Was ist der Unterschied zwischen THF und Dioxan?
Sowohl THF als auch Dioxan sind organische Lösungsmittel, die für die Analyse von Proben wichtig sind. Der Schlüsselunterschied zwischen THF und Dioxan besteht darin, dass THF -Moleküle ein Sauerstoffatom als Mitglied der Ringstruktur enthalten, während das Dioxanmolekül zwei Sauerstoffatome als Mitglieder der Ringstruktur enthält. Wir können Dioxan als Ersatz für THF aufgrund von geringer Toxizität und hohem Siedepunkt verwenden.
Die folgende Infografik zeigt mehr Details zum Unterschied zwischen THF und Dioxan.

Zusammenfassung -THF gegen Dioxan
Sowohl THF als auch Dioxan sind organische Lösungsmittel, die für die Analyse von Proben wichtig sind. Der Schlüsselunterschied zwischen THF und Dioxan besteht darin, dass THF -Moleküle ein Sauerstoffatom als Mitglied der Ringstruktur enthalten, während das Dioxanmolekül zwei Sauerstoffatome als Mitglieder der Ringstruktur enthält.
Referenz:
1. “1,4-Dioxan.Wikipedia, Wikimedia Foundation, 9. September. 2020, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Tetrahydrofuran Probe" von Lhchem - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia
2. "1-4-dioxan" von Rhododendronbusch-eigene Arbeit (Public Domain) über Commons Wikimedia


