Was ist der Unterschied zwischen der Phosphorylgruppe und der Phosphatgruppe
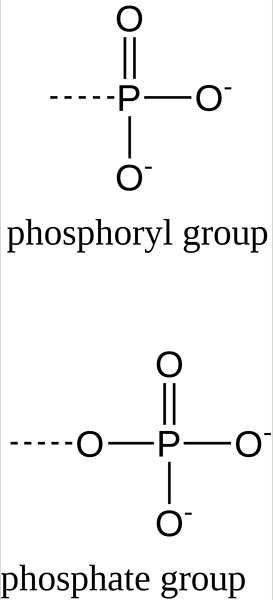
Der Schlüsselunterschied zwischen Phosphorylgruppe und Phosphatgruppe ist diese Phosphorylgruppe enthält ein an drei Sauerstoffatome gebundener Phosphor -Atom und -2 -Ladung, während die Phosphatgruppe ein an vier Sauerstoffatome gebundener Phosphoratom enthält und -3 Ladung.
Die Phosphorylgruppe ist ein chemisches Ion mit der chemischen Formel P+Ö32- Während die Phosphatgruppe ein Anion mit der chemischen Formel PO ist4-3.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Phosphorylgruppe
3. Was ist Phosphatgruppe
4. Phosphorylgruppe gegen Phosphatgruppe in tabellarischer Form
5. Zusammenfassung -Phosphorylgruppe gegen Phosphatgruppe
Was ist Phosphorylgruppe?
Die Phosphorylgruppe ist ein chemisches Ion mit der chemischen Formel P+Ö32-. Daher enthält dieses Ion Phosphor- und Sauerstoffatome. Es kann in verschiedenen Protonierungszuständen existieren. Dieser Begriff wird hauptsächlich für chemische Verbindungen verwendet, die aus einer Phosphorylgruppe bestehen, die an ein anderes Atom gebunden ist, z. Dieser Begriff ist auch nützlich, um katalytische Mechanismen wie Phosphorylierung zu beschreiben.
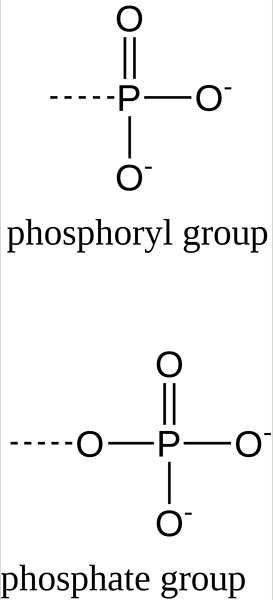
Abbildung 01: Die chemische Formel der Phosphorylgruppe und der Phosphatgruppe
Bei der Betrachtung der biochemischen Prozesse wird eine Phosphorylgruppe normalerweise zwischen den Substratverbindungen übertragen, wenn eine Phosphatgruppe an einer Reaktion beteiligt ist. Diese Reaktionen werden als Phosphorylübertragungsreaktionen bezeichnet. Eine Phosphorylgruppe ist jedoch keine Phosphatgruppe.
Was ist Phosphatgruppe?
Eine Phosphatgruppe ist ein Anion mit der chemischen Formel PO4-3. Dieser Begriff kann verwendet werden, um Am -Anionen, Salzverbindungen zu nennen, die die Phosphatgruppe enthalten, eine funktionelle Gruppe und die Ester, die die Phosphatgruppe enthalten. Am häufigsten nennen wir dieses Anion ein Orthophosphatanion, weil es sich aus Orthophosphorsäure bildet.
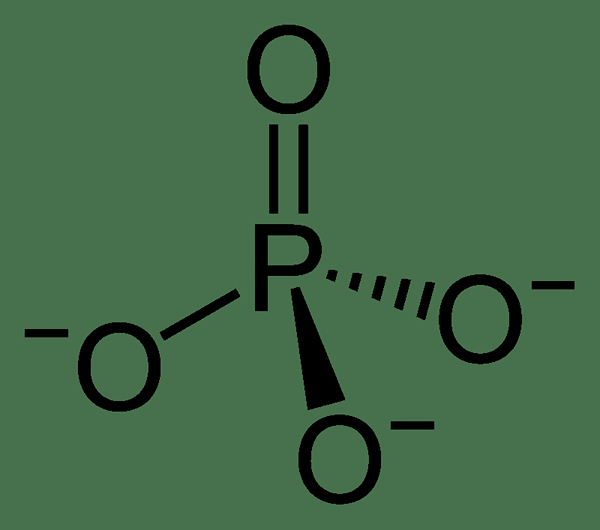
Abbildung 02: Die chemische Struktur der Phosphatgruppe
Dieses Anion bildet sich aus Phosphorsäure durch die Entfernung von drei Protonen. Die Entfernung eines Protons bildet Dihydrogenphosphatanion, während die Entfernung von zwei Protonen Wasserstoffphosphatanion bildet. Diese Namen können verwendet werden, um auf ihre entsprechenden Salzverbindungen zu verweisen.
Die Molmasse von Phosphatanion beträgt 94.97 g/mol. Es gibt ein zentrales Phosphoratom, das an vier Sauerstoffatome gebunden ist, und das Anion hat eine tetraedrische Geometrie. Die meisten phosphathaltigen Verbindungen sind wasserlösliche Substanzen bei Raumtemperatur und Druck. Einige Phosphatverbindungen sind auch in Wasser unlöslich.
In biologischen Systemen können wir hauptsächlich Phosphatgruppen in anorganischer Phosphatform finden. Wir können freie Phosphatanionen in Lösungen in biologischen Systemen finden. Wenn nicht, treten die Phosphatanionen in Form von Organophosphaten an organische Moleküle auf. In der Regel können Phosphate als Ester in Nukleotiden, in DNA und in RNA gefunden werden.
Was ist der Unterschied zwischen der Phosphorylgruppe und der Phosphatgruppe?
Die Phosphorylgruppe ist ein chemisches Ion mit der chemischen Formel p+Ö32- Während die Phosphatgruppe ein Anion mit der chemischen Formel PO ist4-3. Der Schlüsselunterschied zwischen der Phosphorylgruppe und der Phosphatgruppe besteht darin, dass die Phosphorylgruppe ein Phosphor -Atom enthält, das an drei Sauerstoffatome und -2 -Ladungen gebunden ist, während die Phosphatgruppe ein Phosphoratom enthält, das an vier Sauerstoffatome und -3 Ladung gebunden ist.
Die folgende Abbildung zeigt den Unterschied zwischen Phosphorylgruppe und Phosphatgruppe in tabellarischer Form.
Zusammenfassung -Phosphorylgruppe gegen Phosphatgruppe
Eine Phosphorylgruppe ist ein chemisches Ion mit der chemischen Formel p+Ö32-. Inzwischen ist die Phosphatgruppe ein Anion mit der chemischen Formel PO4-3. Der Schlüsselunterschied zwischen der Phosphorylgruppe und der Phosphatgruppe besteht darin, dass die Phosphorylgruppe ein Phosphor -Atom enthält, das an drei Sauerstoffatome und -2 -Ladungen gebunden ist, während die Phosphatgruppe ein Phosphoratom enthält, das an vier Sauerstoffatome und -3 Ladung gebunden ist.
Referenz:
1. „Phosphatgruppe: Definition und Erklärung.” Lernen.com.
Bild mit freundlicher Genehmigung:
1. "Phosphorylgruppe und -phosphatgruppe" durch Strater-erzeugt mit Chemdraw (CC BY-SA 3.0) über Commons Wikimedia
2. "Phosphat -Ion" von Neurotiker ⇌ - eigene Arbeit (Public Domain) über Commons Wikimedia


