Unterschied zwischen Edelgaskonfiguration und Elektronenkonfiguration
Der Schlüsselunterschied Zwischen der Konfiguration von Nobelgas und der Elektronenkonfiguration befindet sich das A Die Edelgaskonfiguration verfügt nur über Elektronenpaare, während eine Elektronenkonfiguration sowohl gepaarte als auch ungepaarte Elektronen haben kann.
Der Begriff Elektronenkonfiguration bezieht sich auf die Elektronensequenz oder die Reihenfolge der in einem Atom eines bestimmten chemischen Elements vorhandenen Elektronen. Der Begriff Edelgaselektronenkonfiguration zeigt an, dass alle Atomorbitale vollständig mit Elektronen gefüllt sind.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist die Konfiguration von Noble Gas
3. Was ist die Elektronenkonfiguration
4. Seite für Seite Vergleich - Noble Gaskonfiguration im Vergleich zur Elektronenkonfiguration in tabellarischer Form
5. Zusammenfassung
Was ist die Konfiguration von Noble Gas?
Edelgaskonfiguration ist die Elektronenkonfiguration eines edlen Gasatoms. Die edlen Gasatome sind die Atome der chemischen Elemente der Gruppe 18 im Periodensystem. Die chemischen Elemente der Gruppe 18 sind aus zwei Gründen als Edelgaselemente bekannt; Erstens sind diese chemischen Elemente aufgrund ihrer abgeschlossenen Elektronenkonfigurationen größtenteils nicht reaktiv, und der zweite Grund ist, dass diese chemischen Elemente in der gasförmigen Phase in der Natur auftreten.

Abbildung 01: Verschiedene edle Gase
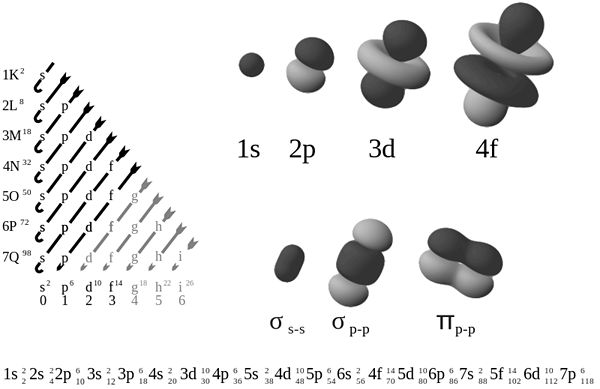
Es gibt vier Haupttypen von Atomorbitalen in einem chemischen Element; S Orbital, P Orbital, D Orbital und F Orbital. Das S -Atom -Orbital enthält maximal zwei Elektronen, das P -Orbital kann sechs Elektronen enthalten, D Orbital kann zehn Elektronen halten und das F -Orbital kann 14 Elektronen halten. In der Gruppe 18 chemische Elemente können wir die S2p6 -Elektronenkonfiguration beobachten. Hier sind die S- und P -Atomorbitale vollständig mit Elektronen gefüllt. Daher gibt es in diesen Atomen keine ungepaarten Elektronen.
Was ist die Elektronenkonfiguration?
Die Elektronenkonfiguration ist die Verteilung der Elektronen eines Atoms in den Atomorbitalen. Dieser Begriff beschreibt jedes Elektron im Atom als unabhängig in einem Orbital in einem durchschnittlichen Feld, das von allen anderen Orbitalen erstellt wurde.
Die Elektronenkonfiguration eines Atom. Einige chemische Elemente wie Edelgasatome haben atomare Orbitale abgeschlossen, und es gibt keine ungepaarten Elektronen; Die meisten chemischen Elemente, die wir kennen, haben jedoch ungepaarte Elektronen in ihrer Elektronenkonfiguration. Beispielsweise hat die Elektronenkonfiguration von Neon Atom, einem edlen Gasatom, die Elektronenkonfiguration 1s22s22p6.

Durch die Betrachtung der Elektronenkonfiguration eines Atoms können wir die Reaktivität dieses Atoms beschreiben. Ein vollständig gefülltes atomares Orbital zeigt eine nicht respektive Natur an, da es keine Elektronen mehr erhalten muss, um sich selbst zu stabilisieren. Im Gegensatz dazu sind in einem Atom mit ungepaarten Elektronen häufig hochreaktiv, um ihre Elektronenkonfiguration zu stabilisieren.
Was ist der Unterschied zwischen der Konfiguration von Edelgas und der Elektronenkonfiguration?
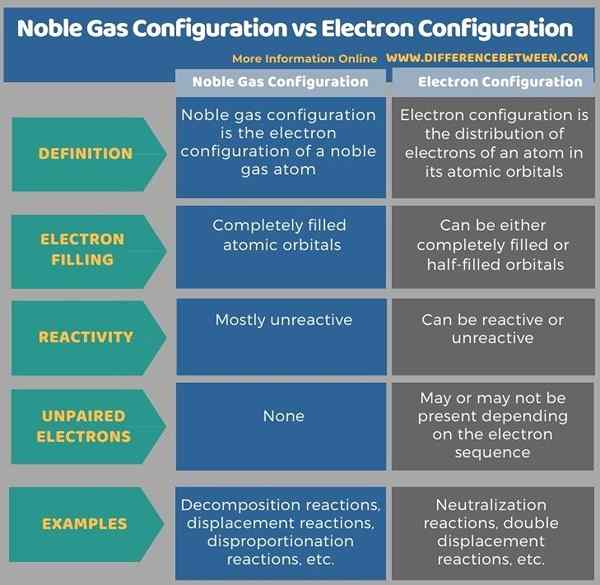
Noble Gaskonfiguration ist die Elektronenkonfiguration eines edlen Gasatoms. Das bedeutet, dass das Atom atomare Orbitale vollständig gefüllt hat. Der wichtigste Unterschied zwischen der Konfiguration der Edelgas und der Elektronenkonfiguration besteht darin, dass die Noble -Gas -Konfiguration nur Elektronenpaare aufweist, während eine Elektronenkonfiguration sowohl gepaarte als auch ungepaarte Elektronen haben kann. Das bedeutet; Die Edelgaskonfiguration hat die Atomorbitale vollständig gefüllt, während die Elektronenkonfiguration entweder vollständig gefüllte oder halb gefüllte Orbitale haben kann.
Nachfolgend Infografik listet mehr Unterschiede zwischen der Konfiguration der Edelgas und der Elektronenkonfiguration auf.
Zusammenfassung -Konfiguration von Noble Gas im Vergleich zur Elektronenkonfiguration
Eine Elektronenkonfiguration ist die Abfolge von Elektronen, die in einem Atom vorhanden sind. Der wichtigste Unterschied zwischen der Konfiguration der Edelgas und der Elektronenkonfiguration besteht darin, dass die Noble -Gas -Konfiguration nur Elektronenpaare aufweist, während eine Elektronenkonfiguration sowohl gepaarte als auch ungepaarte Elektronen haben kann.
Referenz:
1. „Noble Gas.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 23. Oktober. 2020, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Glühende edle Gase" von New Work Alchemist-HP (Talk) www.Pse-Mendelejew.de); Original einzelne Bilder: Jurii, http: // Bilder von Elementen.com. - Original: Jurii (CC von 3.0) über Commons Wikimedia
2. "Elektronenorbitale" von Patricia.FIDI - eigene Arbeit von Patricia.Fidi und Lt Paul - Ursprünglich aus PL: Grafika: Orbitale.PNG, Autor PL: Wikipedysta: Chemmix.Diese W3C- (Public Domain) über Commons Wikimedia


