Was ist der Unterschied zwischen Ethanol und Methoxymethan

Der Schlüsselunterschied zwischen Ethanol und Methoxymethan ist, dass Ethanol als farblose Flüssigkeit auftritt, die bei Raumtemperatur stark flüchtig ist, während Methoxymethan als farbloses Gas bei Raumtemperatur auftritt.
Ethanol und Methoxymethan haben die gleiche chemische Formel, aber unterschiedliche chemische Strukturen, die die verschiedenen chemischen Eigenschaften dieser Verbindungen bestimmt. Ethanol oder Ethylalkohol ist eine organische Verbindung mit der chemischen Formel C2H5OH. Methoxymethan ist eine Ätherverbindung mit der chemischen Formel C2H6Ö.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Ethanol
3. Was ist Methoxymethan
4. Ethanol gegen Methoxymethan in tabellarischer Form
5. Zusammenfassung -Ethanol gegen Methoxymethan
Was ist Ethanol?
Ethanol oder Ethylalkohol ist eine organische Verbindung mit der chemischen Formel C2H5OH. Es ist nützlich als Kraftstoff. Es ist jedoch dieselbe Verbindung, die wir in alkoholischen Getränken finden. Meistens wird dieser Kraftstoff als Motorkraftstoff als Biokraftstoff -Additiv für Benzin verwendet.

Abbildung 01: Eine Flasche Ethanol
Es ist möglich, Ethanol über biologische oder chemische Mittel zu produzieren. Die Hauptschritte zur Herstellung von Ethanol über biologische Mittel sind Fermentation, Destillation und Dehydration. Während der Fermentation wirken Mikroben auf Zucker, um es in Ethanol umzuwandeln. Der Destillationsschritt umfasst die Entfernung von Mikroben und den größten Teil des Wassers. Dort ist das Produkt der Fermentation erhitzt, sodass die Ethanolfraktion verdunstet. Danach sollten wir das Endprodukt der Destillation dehydrieren, um einen äußerst reinen Bruchteil von Ethanol zu erhalten. Darüber hinaus umfasst die Produktion von Ethanol über chemische Mittele die Reaktion von Ethen mit Dampf.
Was ist Methoxymethan?
Methoxymethan ist eine Ätherverbindung mit der chemischen Formel C2H6Ö. Der gebräuchliche Name dieser Verbindung ist Dimethylether. Diese Verbindung ist bekannt für ihre Lösungsmitteleigenschaften. Es hat zwei Methylgruppen, die über ein Sauerstoffatom gebunden sind; Die beiden Methylgruppen sind an dasselbe Sauerstoffatom gebunden.
Die Molmasse von Methoxymethan beträgt 46.07 g/mol. Der Schmelzpunkt dieser Substanz beträgt -141 Celsius Grad, während der Siedepunkt -24 Celsius Grad beträgt. Es tritt bei Raumtemperatur als farbloses Gas auf und hat einen ätherähnlichen Geruch. Darüber hinaus ist Dimethylether nicht wasserlöslich.
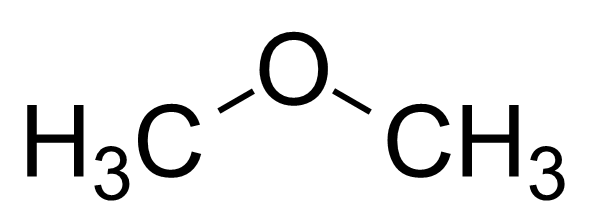
Abbildung 02: Die chemische Struktur von Methoxymethan
Dimethylether ist eine unpolare Verbindung. Dies bedeutet, dass Dimethylether keine Polarität hat. Das liegt an seiner symmetrischen molekularen Struktur. Daher ist es ein gutes Lösungsmittel für nicht-polare Verbindungen. Es ist jedoch im Vergleich zu anderen organischen Verbindungen chemisch unreaktiv.
Was ist der Unterschied zwischen Ethanol und Methoxymethan?
Ethanol und Methoxymethan haben die gleiche chemische Formel, aber unterschiedliche chemische Strukturen, die die verschiedenen chemischen Eigenschaften dieser Verbindungen bestimmt. Der Hauptunterschied zwischen Ethanol und Methoxymethan besteht darin, dass Ethanol als farblose Flüssigkeit auftritt, die bei Raumtemperatur stark flüchtig ist.
Darüber hinaus ist Ethanol ein Alkohol mit einem charakteristischen alkoholischen Geruch, während Methoxymethan ein Ether mit einem ätherischen Geruch ist. Darüber hinaus haben Ethanol und Methoxymethan ähnliche chemische Formeln, die in verschiedenen Strukturen angeordnet sind. Zum Beispiel hat Ethanol eine Hydroxylgruppe (OH -Gruppe), während Methoxymethan keine Hydroxylgruppen hat.
Die folgende Infografik stellt die Unterschiede zwischen Ethanol und Methoxymethan in tabellarischer Form für Seite für Seitenvergleich dar.
Zusammenfassung -Ethanol gegen Methoxymethan
Ethanol oder Ethylalkohol ist eine organische Verbindung mit der chemischen Formel C2H5OH. Methoxymethan ist eine Etherverbindung mit der chemischen Formel C2H6O. Der Hauptunterschied zwischen Ethanol und Methoxymethan besteht darin, dass Ethanol als farblose Flüssigkeit auftritt, die bei Raumtemperatur stark flüchtig ist.
Referenz:
1. "Dimethylether.” Nationales Zentrum für Biotechnologie Information. Pubchem Compound -Datenbank, U.S. Nationalbibliothek für Medizin.
Bild mit freundlicher Genehmigung:
1. "Ethanol-Alkoholschutz-Covid-19" (CC0) über Pixabay
2. "Dimethylether ohne einsame Paare" von B Levin13 - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia


